Acompañamiento Virtual a Estudiantes - Química
- General
General

- IMPORTANTEPara comunicarse con las profesoras envíe un MENSAJEpresionando en el sobrecito que está a la derecha del nombre.
Enlace químico
- Enlace químico
Enlace químico

ENLACE QUÍMICO
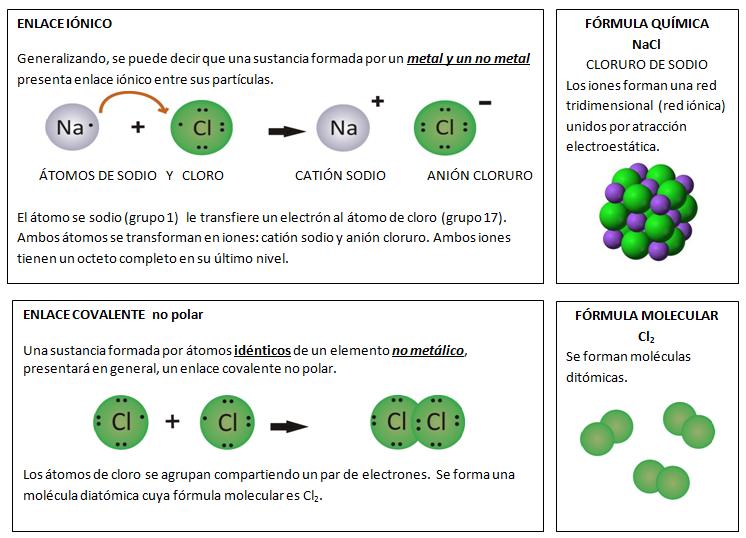
Regla del octeto: los átomos tienden a interaccionar con otros adquiriendo 8 electrones en el nivel más externo de energía, estableciéndose entre ellos un enlace químico.Los metales presentan una tendencia a perder electrones, mientras que los no metales tienden a ganar electrones. De esta manera, básicamente, los átomos adquieren una distribución electrónica más estable, similar a la del gas inerte más próximo en la Tabla Periódica.Se puede realizar las siguientes simplificaciones:• Entre un metal y no metal se transfieren electrones. El metal pierde, el no metal gana. Los átomos pierden su neutralidad eléctrica, transformándose en iones. Entre los iones se establece una fuerza electrostática llamada ENLACE IÓNICO.• Entre átomos de no metales se comparten pares de electrones. Se produce un ENLACE COVALENTE. Esta compartición, en otros casos, no siempre es equitativa:Enlace covalente no polar los pares de electrones están a la misma distancia de los átomos enlazados. Las moléculas formadas por la unión de los átomos son no polares.Enlace covalente polar los pares de electrones no están a la misma distancia de los átomos enlazados. Las moléculas formadas tienen una distribución desigual de los electrones.