GLOSARIO DE QUÍMICA
GLOSARIO DE QUÍMICA
Especial | A | B | C | D | E | F | G | H | I | J | K | L | M | N | Ñ | O | P | Q | R | S | T | U | V | W | X | Y | Z | TODAS
Á |
|---|
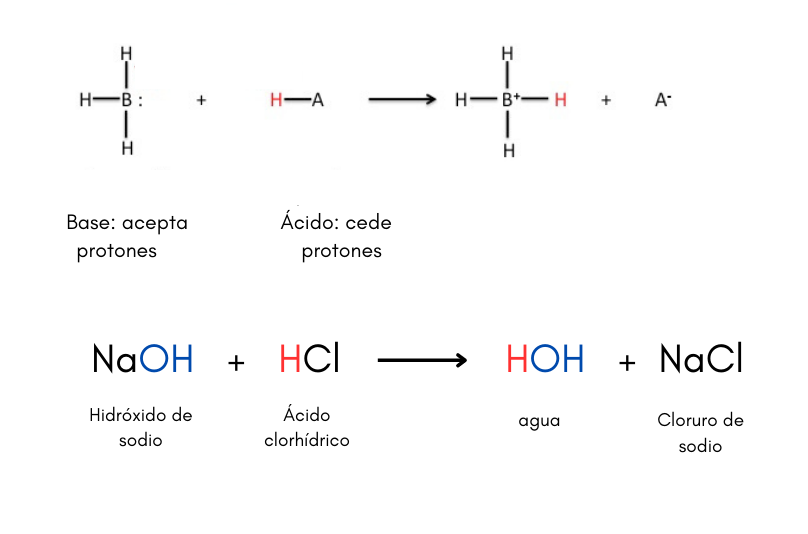
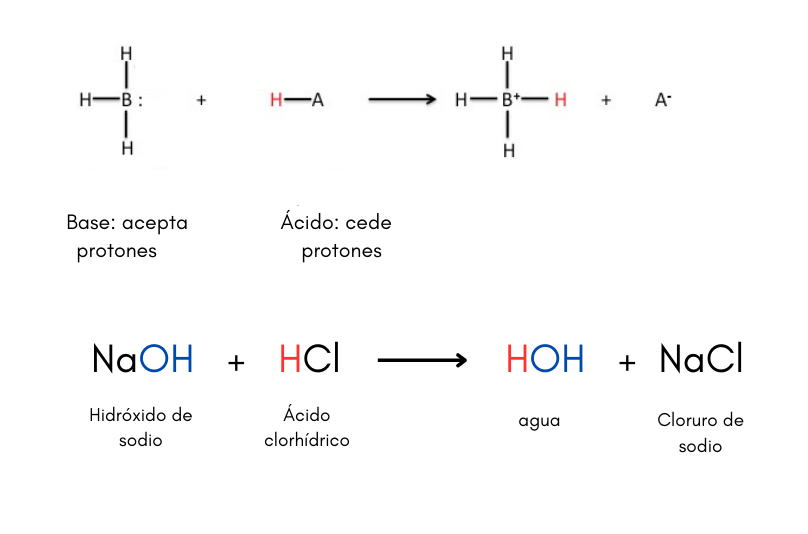
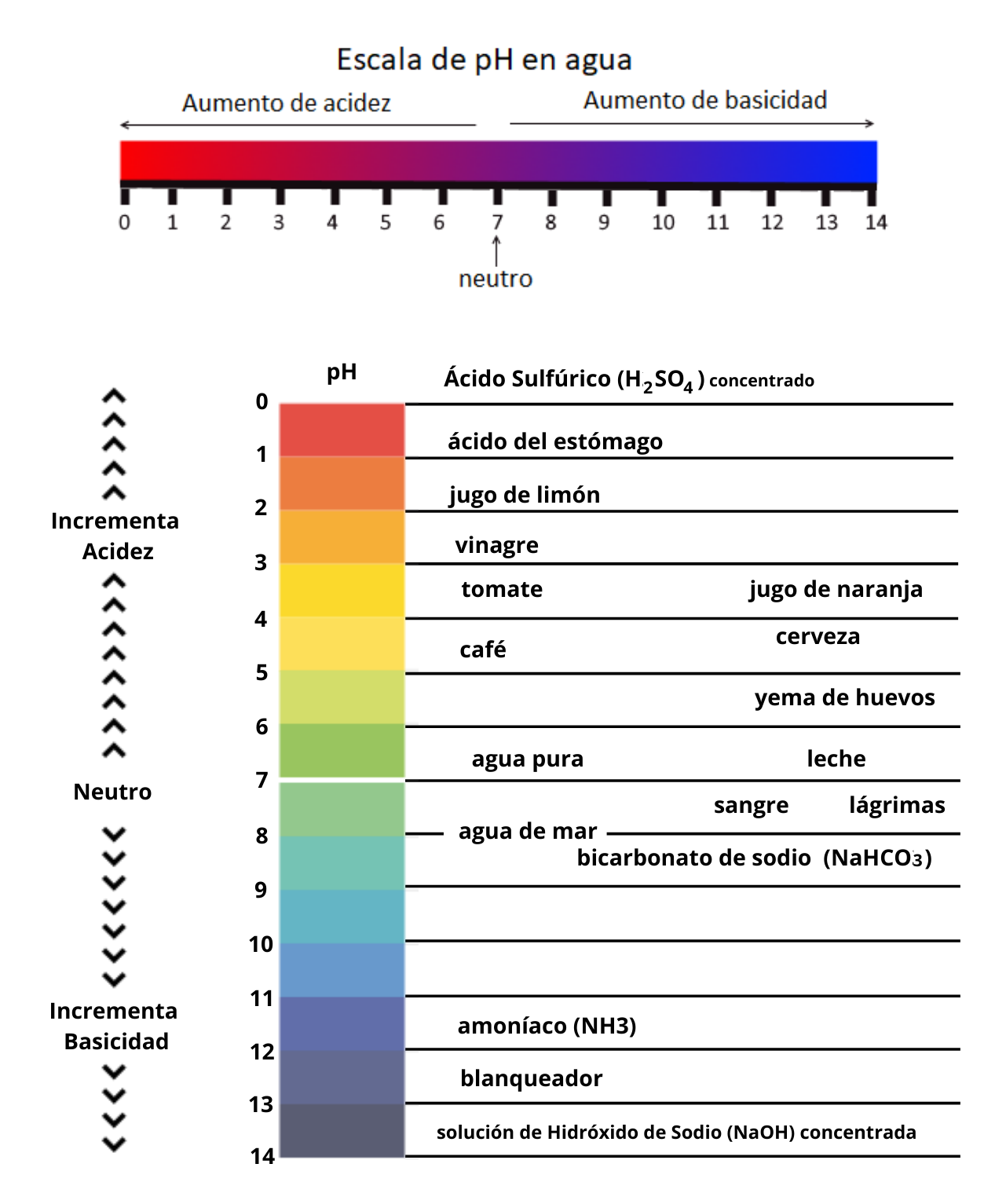
Ácido (teoría de Brönsted-Lowry)Un ácido es una sustancia que puede ceder protones a una base. Por ejemplo:
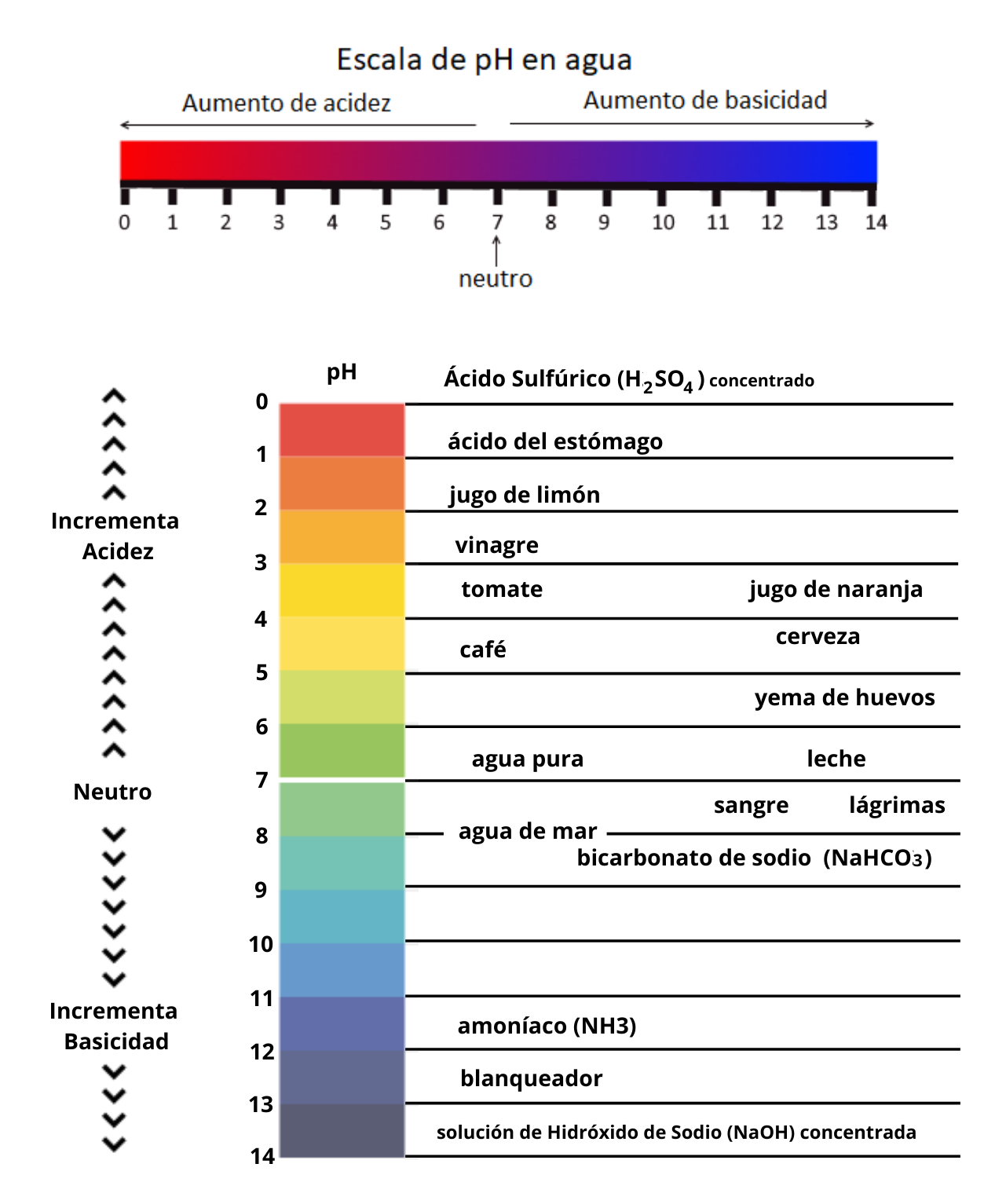
Existen otras teorías de ácidos y bases como por ejemplo la teoría de Lewis. Cuando se disuelve un ácido en agua el valor de pH de la solución es menor que 7.
|
A |
|---|
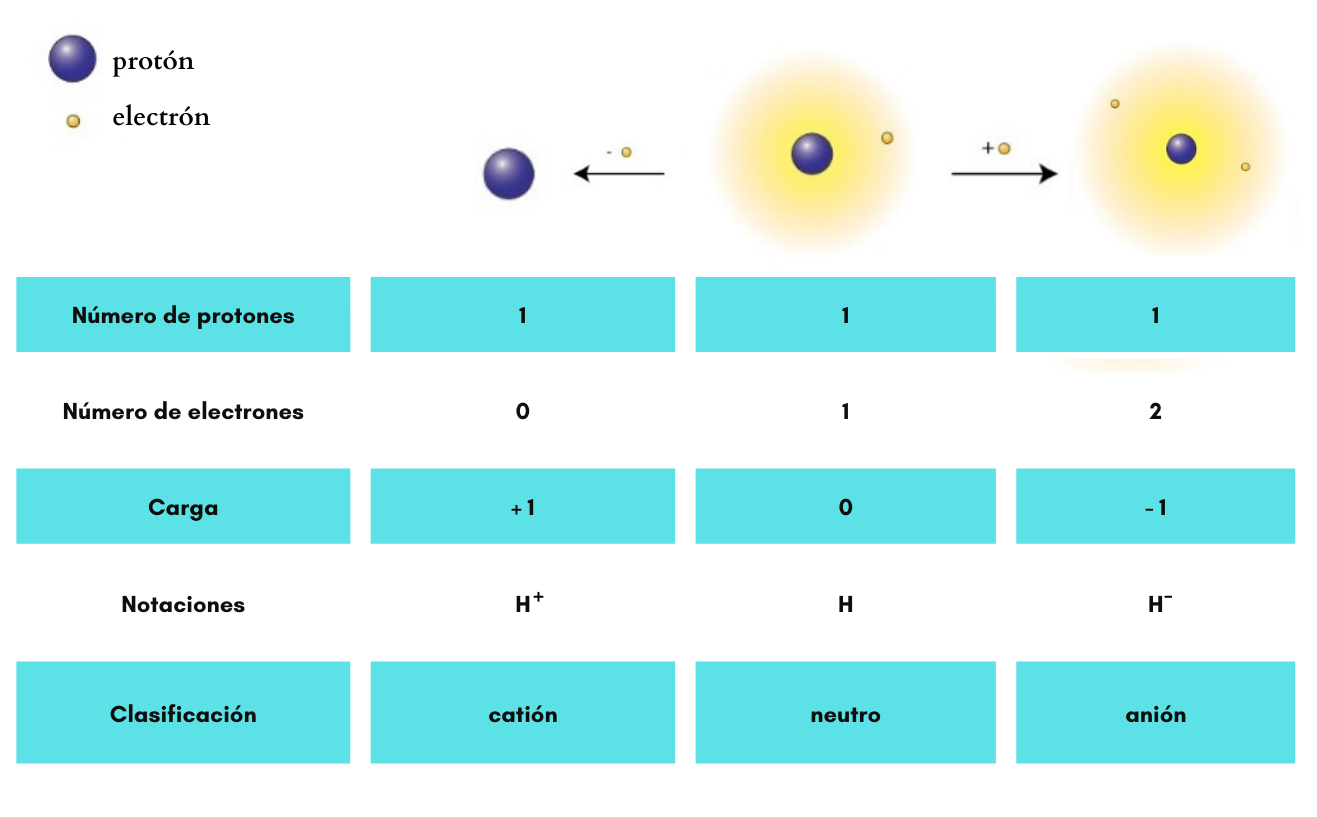
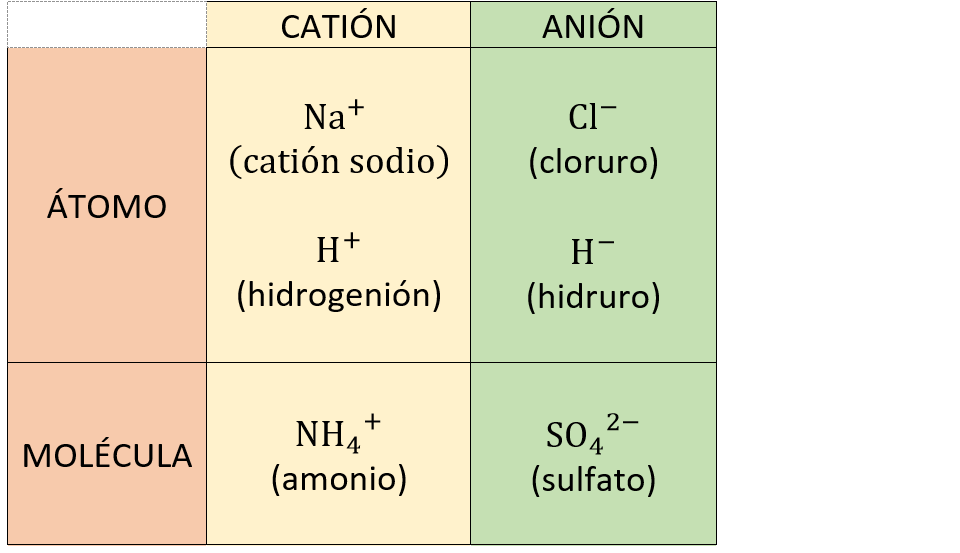
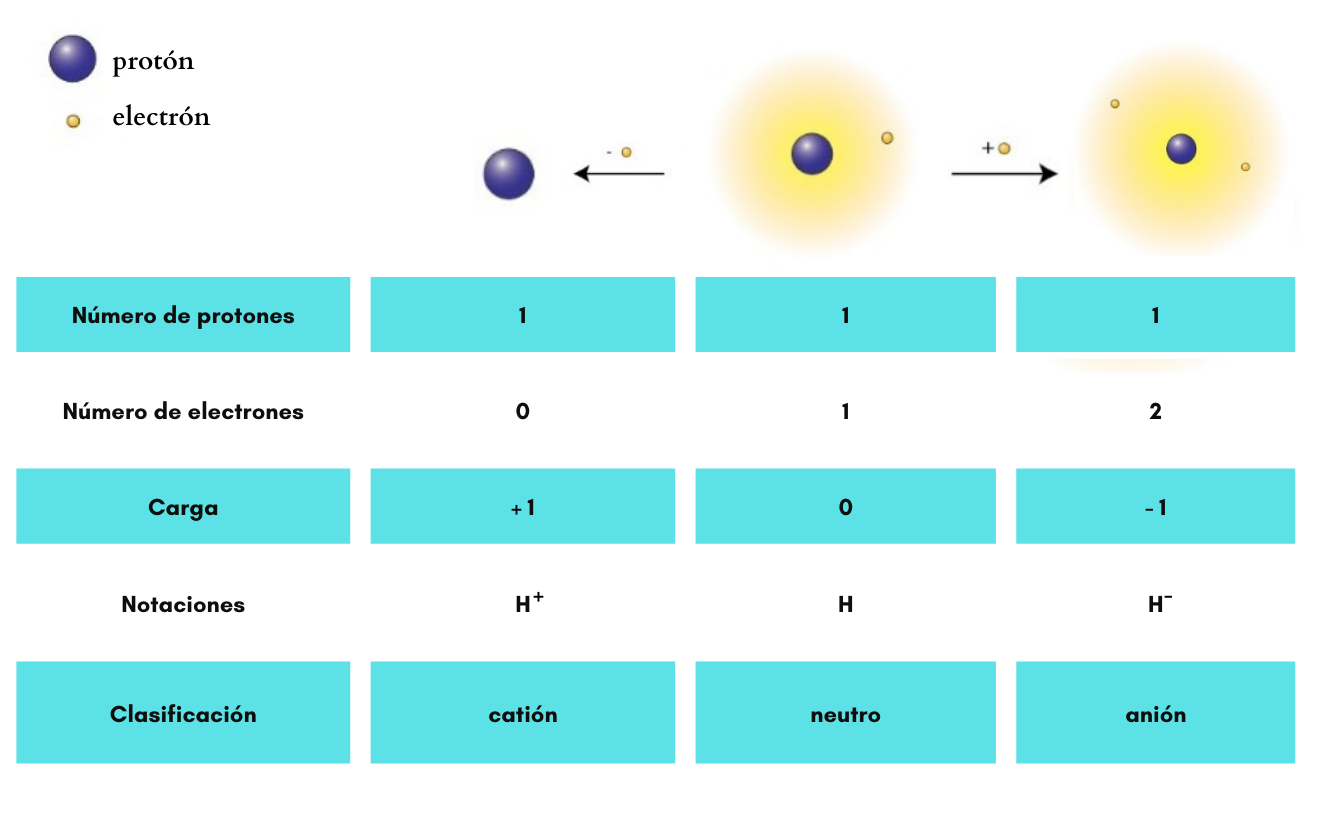
AniónUn
anión es un ion
con
carga eléctrica negativa. Ejemplos:
 |
Á |
|---|
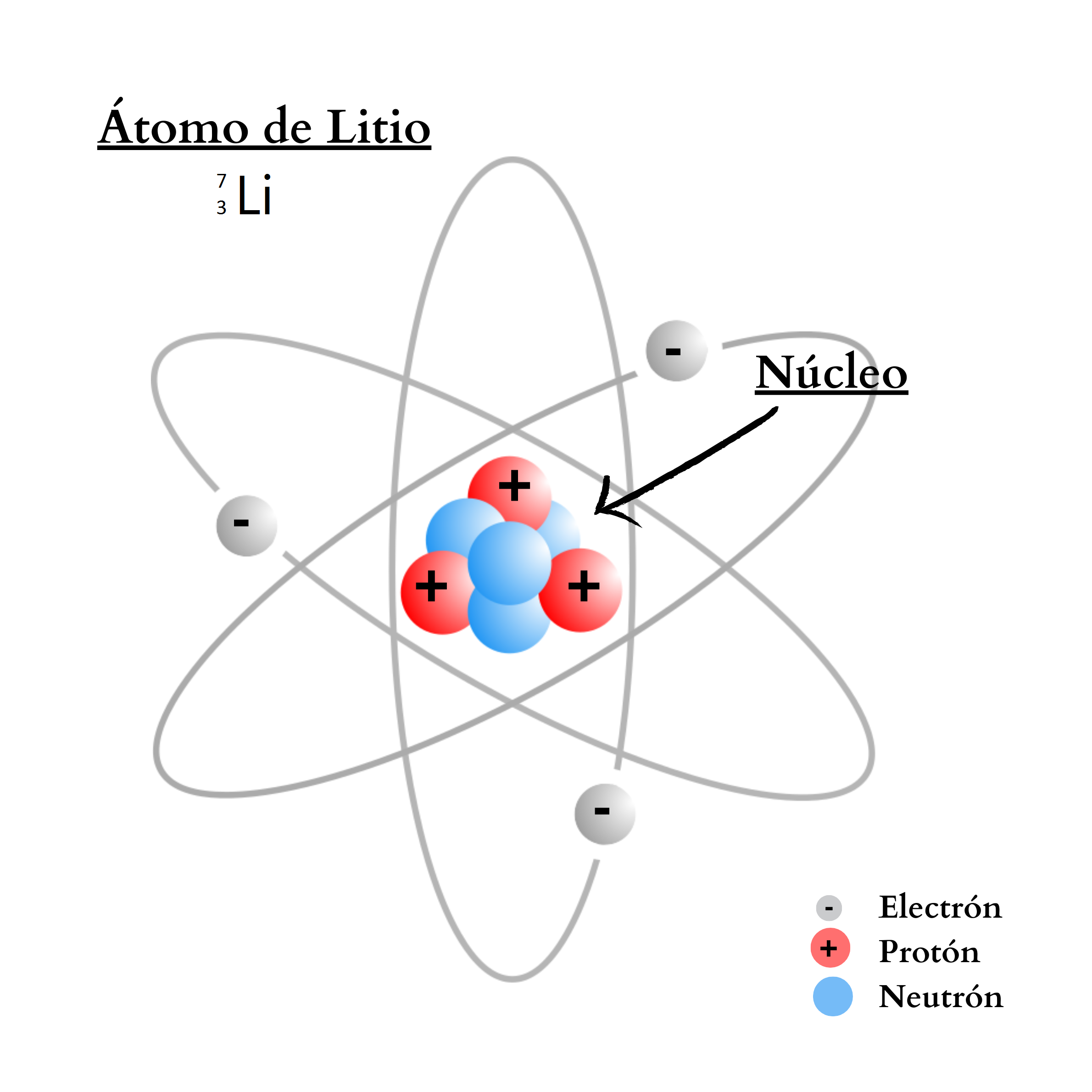
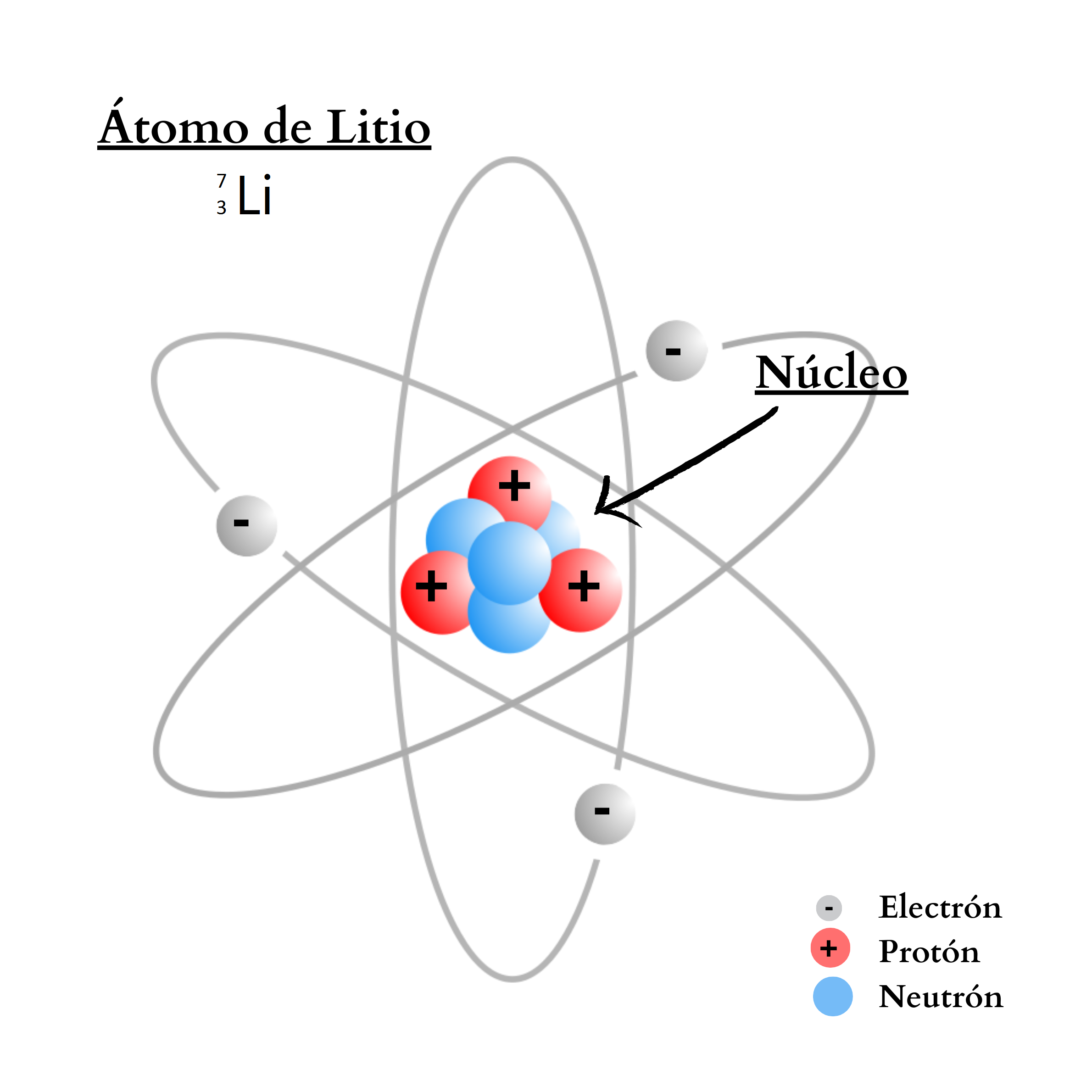
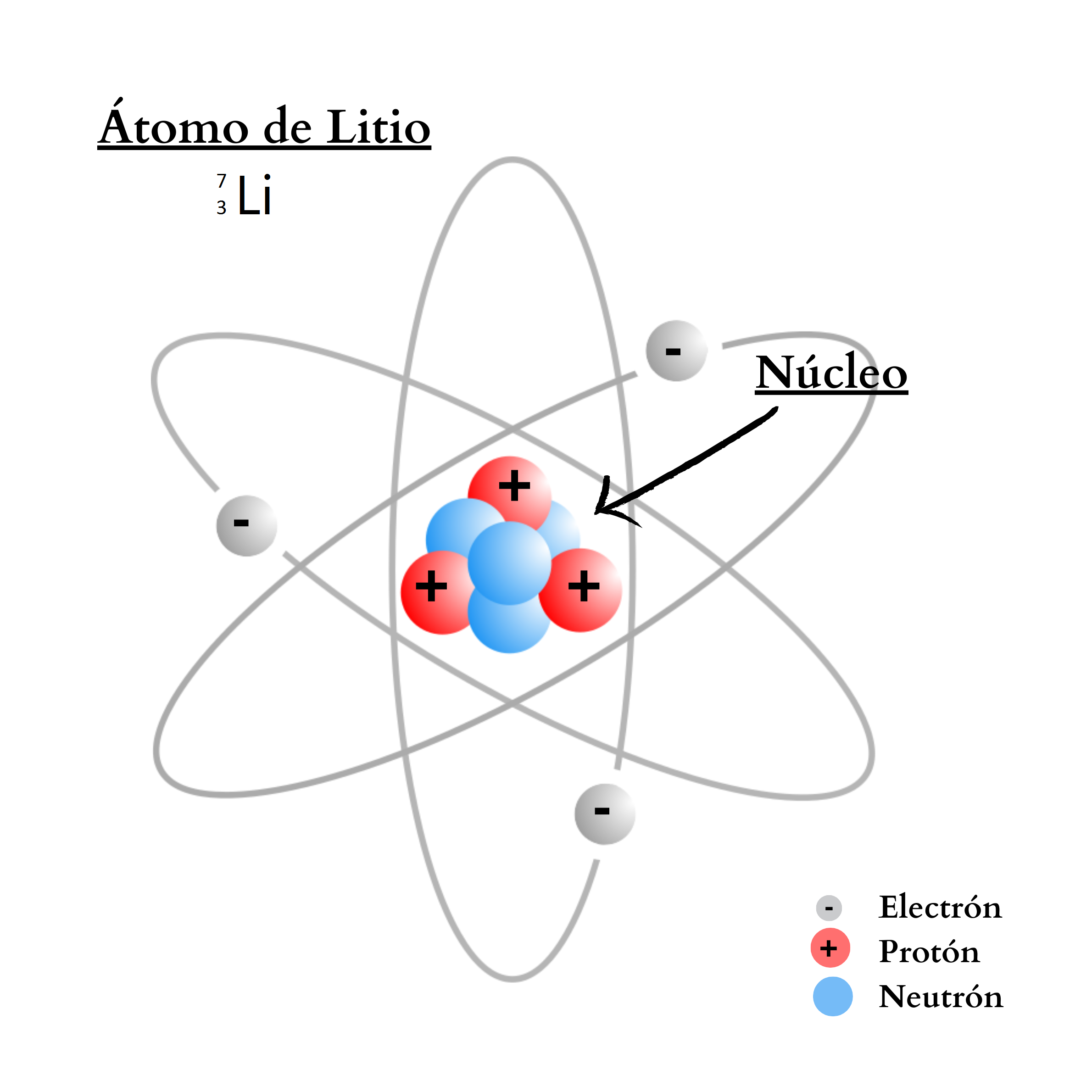
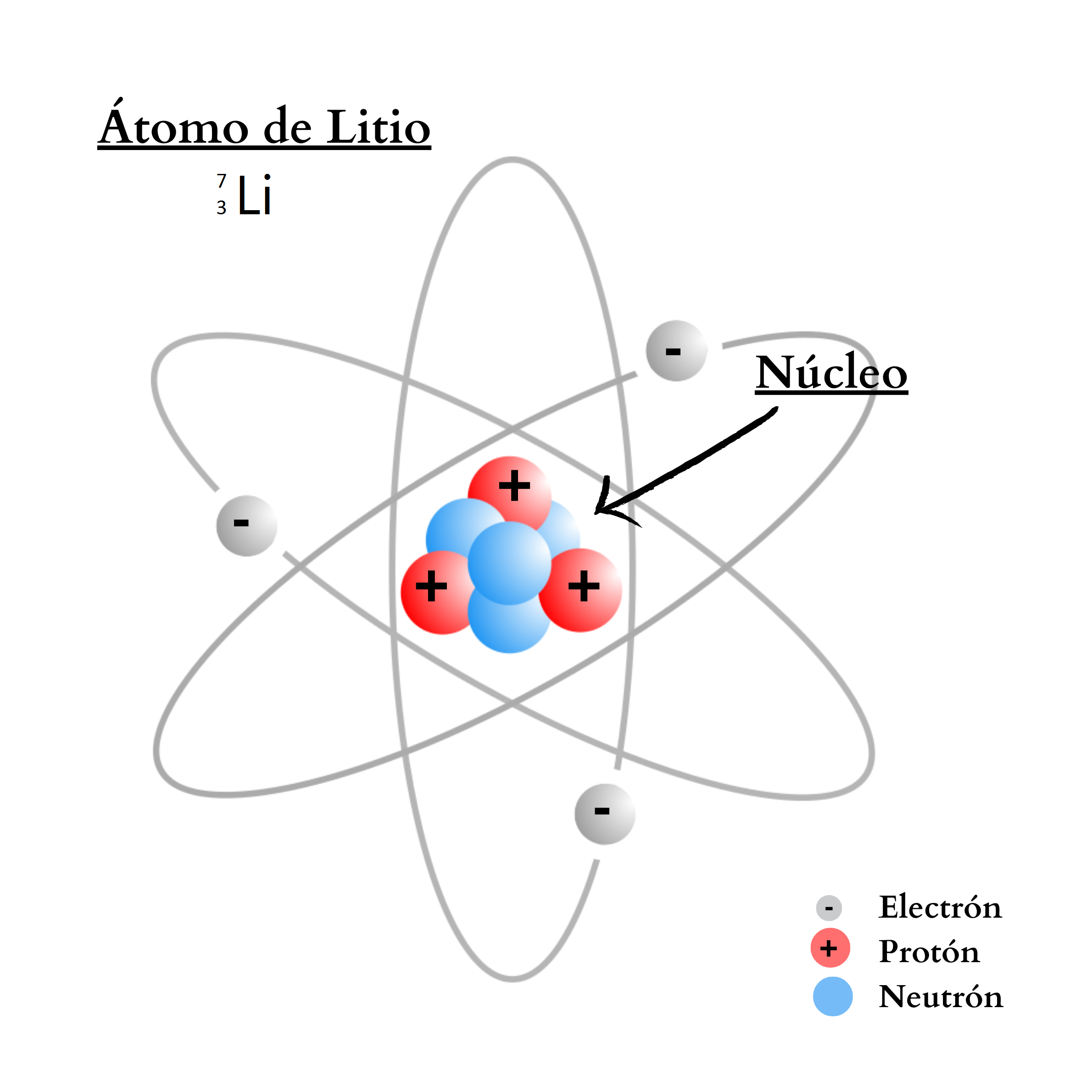
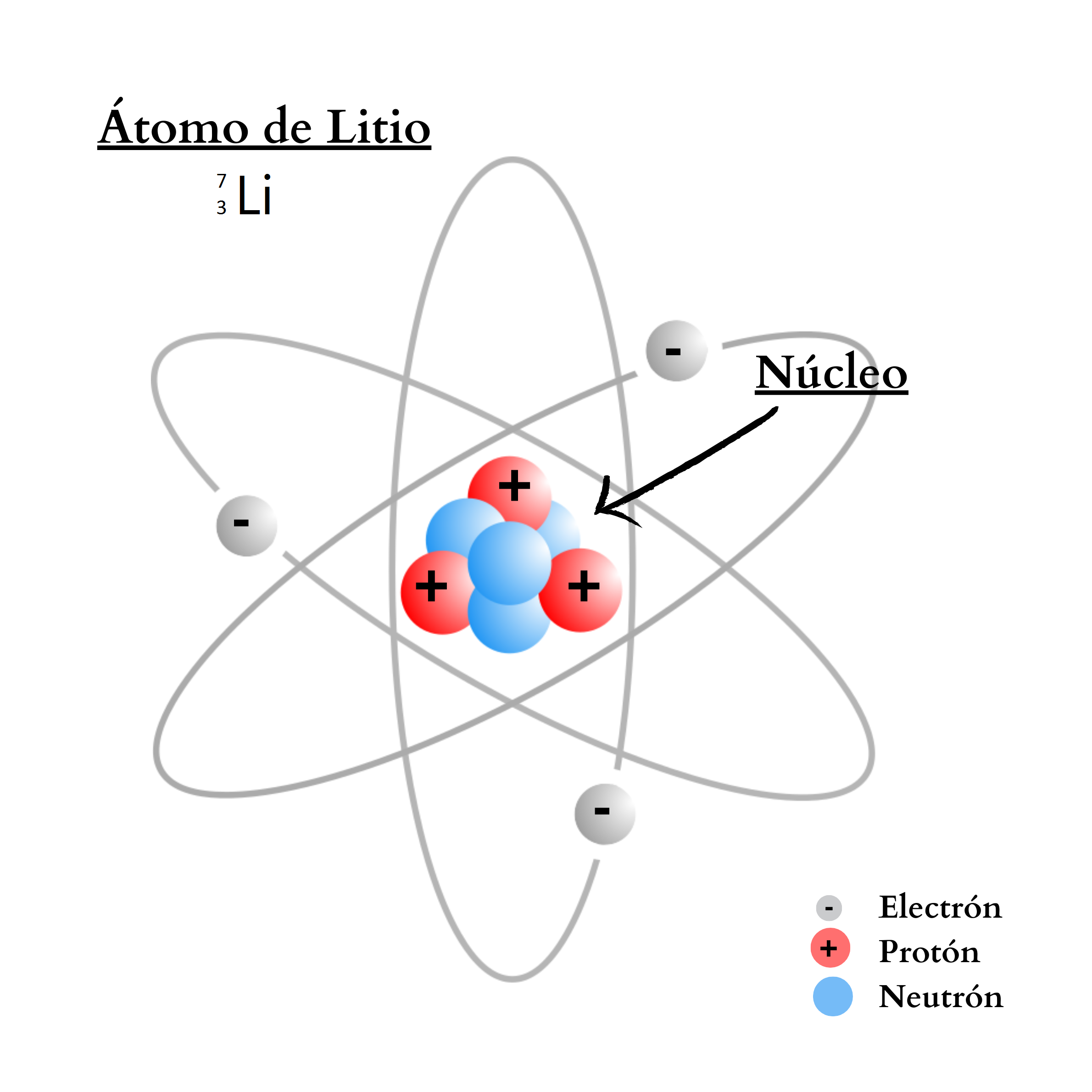
ÁtomoEl átomo es la mínima unidad de la materia que mantiene las propiedades de un elemento químico Un átomo está compuesto por un núcleo y una periferia. En el núcleo del átomo se encuentran los protones y los neutrones. En la periferia se encuentran los electrones. Cada elemento químico se compone de una sola clase de átomos. Cada elemento químico se representa con un símbolo químico formado por una letra o por dos letras. Por ejemplo, el elemento nitrógeno se representa como N, y el elemento calcio como Ca.
|
A |
|---|
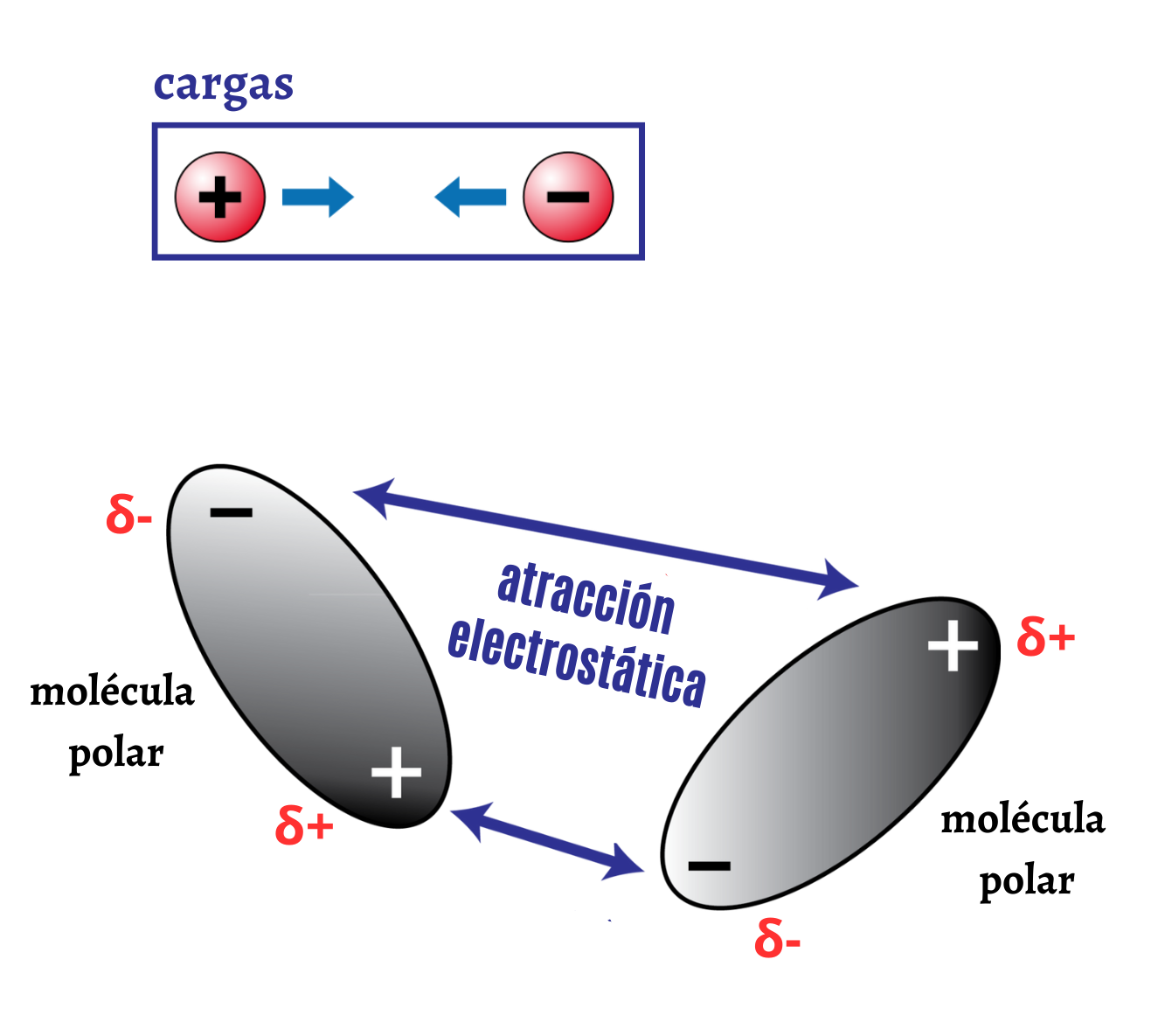
Atracción ElectrostáticaLa atracción electrostática es la interacción entre cargas eléctricas de signo opuesto. La atracción electrostática hace que las cargas de signo opuesto se atraigan. En el caso de moléculas polares la atracción electrostática se establece entre cargas parciales de signo opuesto.
 |
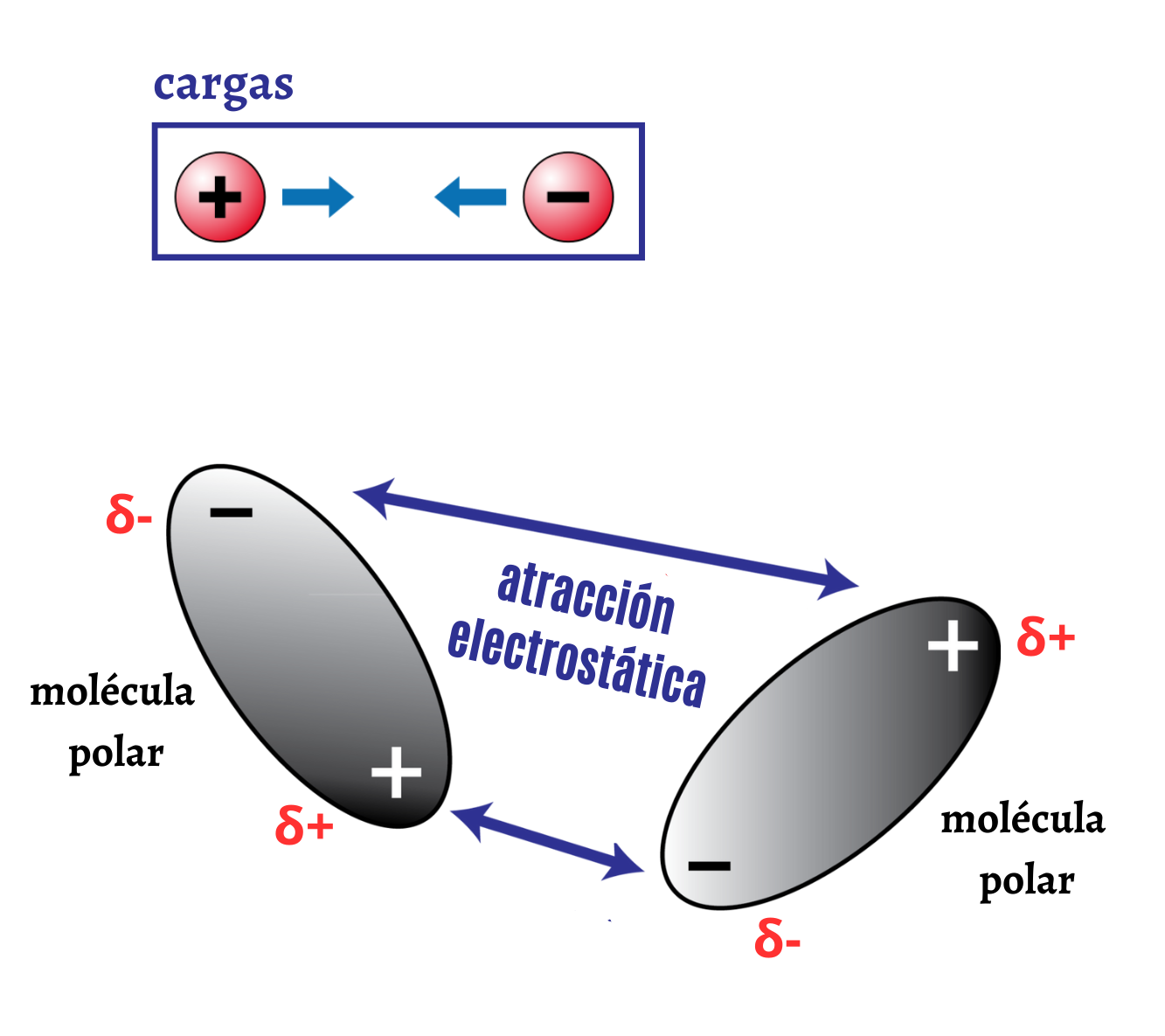
Atracción ElectrostáticaLa atracción electrostática es la interacción entre cargas eléctricas de signo opuesto. La atracción electrostática hace que las cargas de signo opuesto se atraigan. En el caso de moléculas polares la atracción electrostática se establece entre cargas parciales de signo opuesto.
 |
B |
|---|
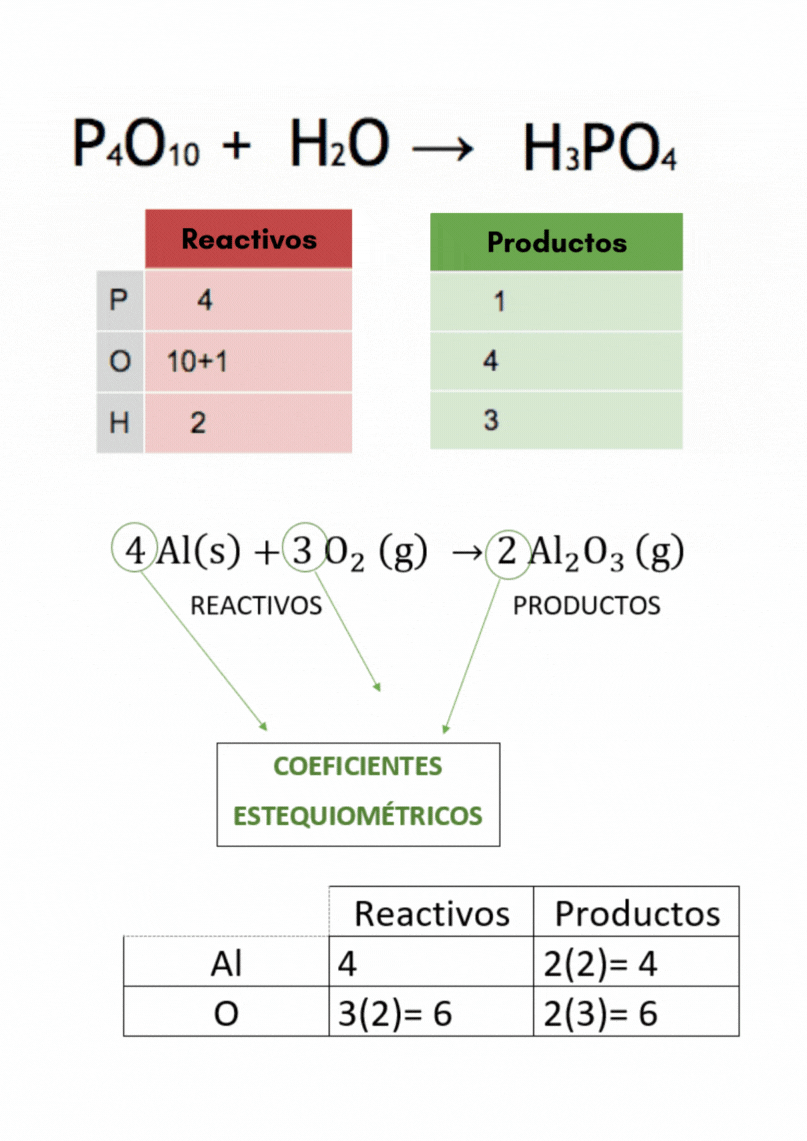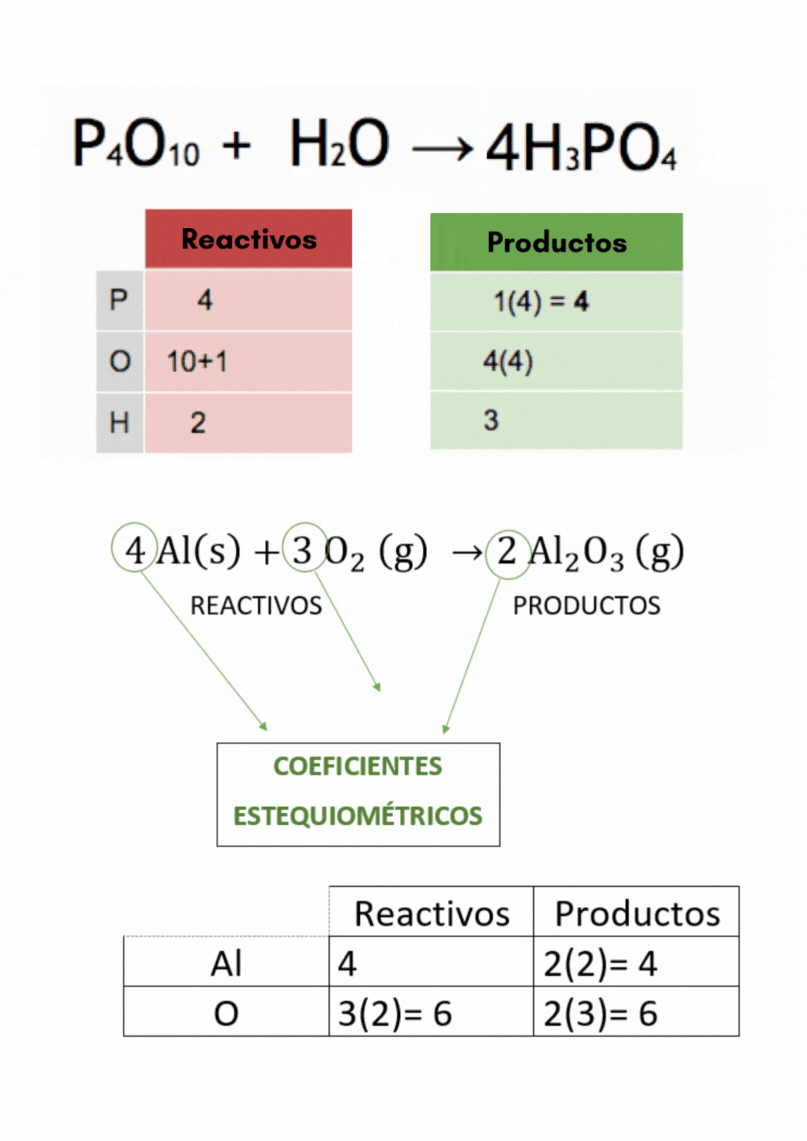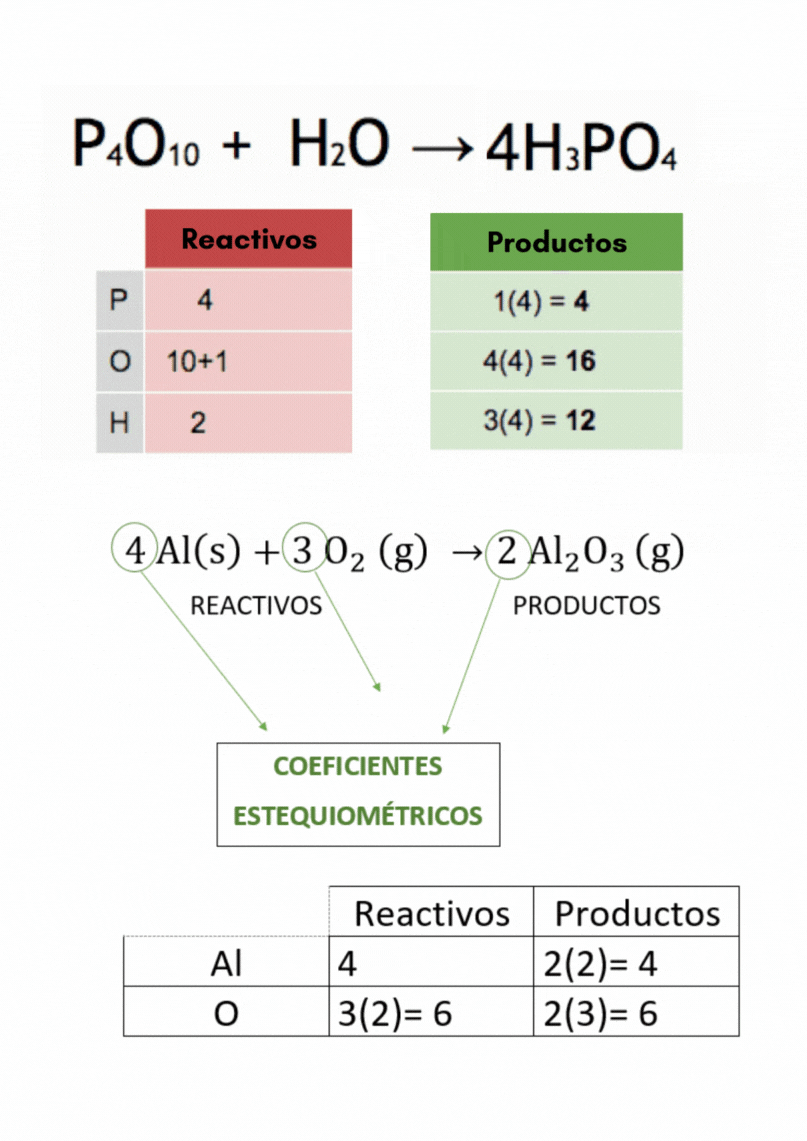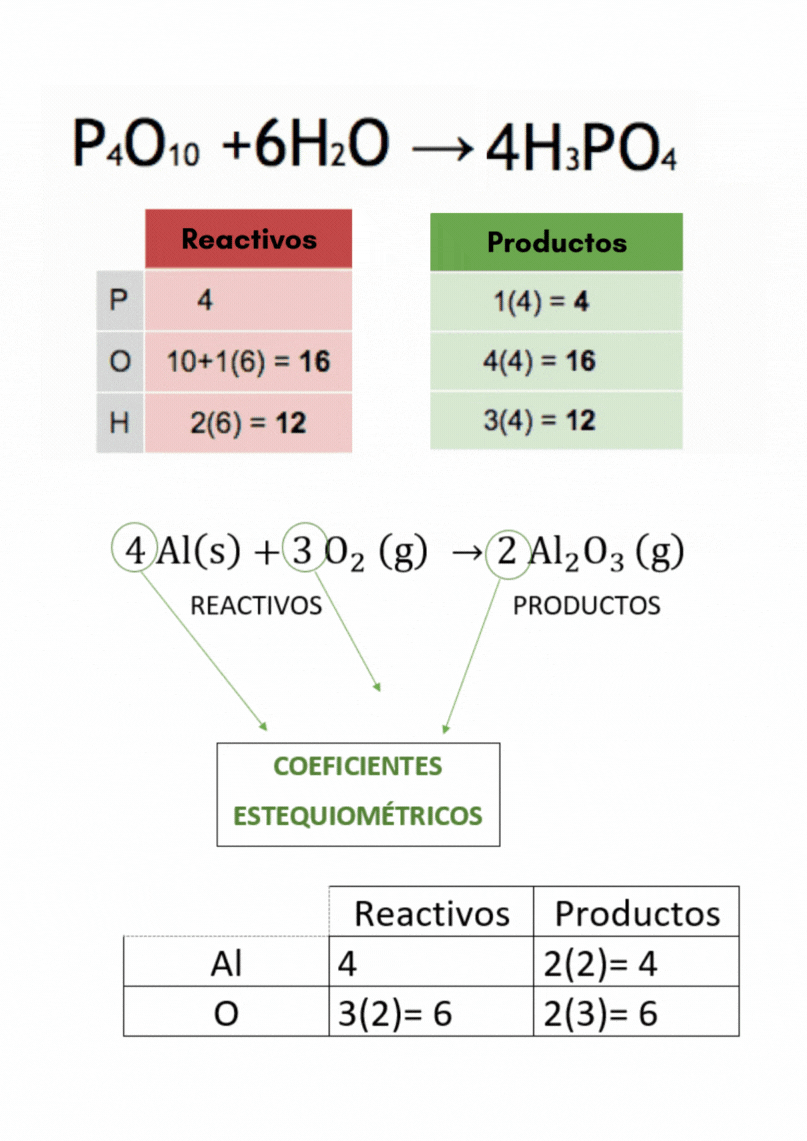
Balanceo o igualación de ecuaciones químicas |
Base (teoría de Brönsted-Lowry)Una base es una sustancia que puede aceptar protones de un ácido. Por ejemplo:
Existen otras teorías de ácidos y bases como por ejemplo la teoría de Lewis. Cuando se disuelve una base en agua el valor de pH de la solución es mayor que 7. Las bases se llaman también álcalis.
|
C |
|---|
Cambio FísicoUn
cambio físico es una transformación en la que no se modifica la
composición
química
de
las sustancias. Un ejemplo de cambio físico es la transformación de hielo en agua líquida. En los dos casos la sustancia es agua (H2O).
|
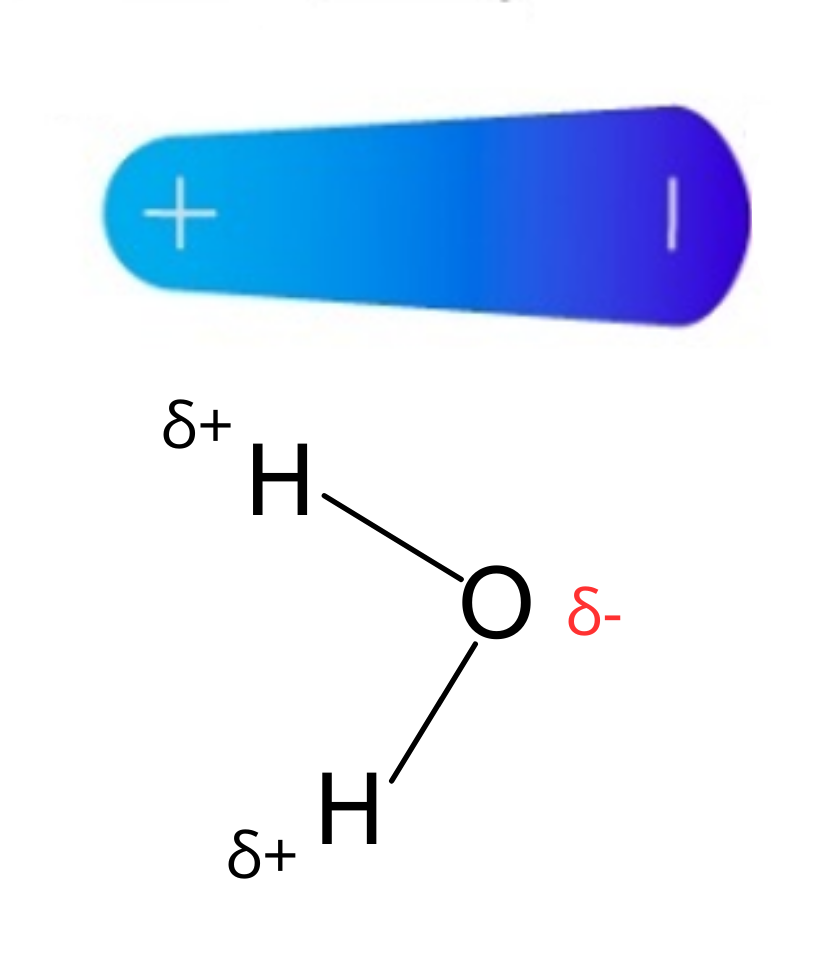
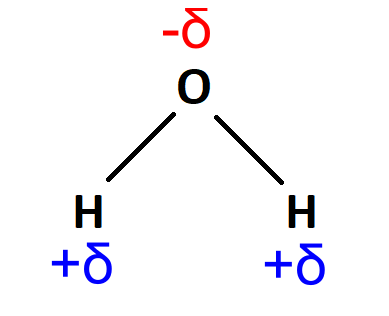
Carga parcialUna carga parcial es una carga eléctrica sobre un átomo. La carga parcial tiene un valor menor a la unidad de carga (1). Las cargas parciales aparecen entre átomos de elementos que tienen diferentes electronegatividades. Las cargas parciales se representan con la letra griega delta (δ) con un signo que indica la carga negativa o positiva: δ− o δ+
 |
CatiónUn
catión es un ion
con
carga eléctrica positiva. Ejemplos:
|
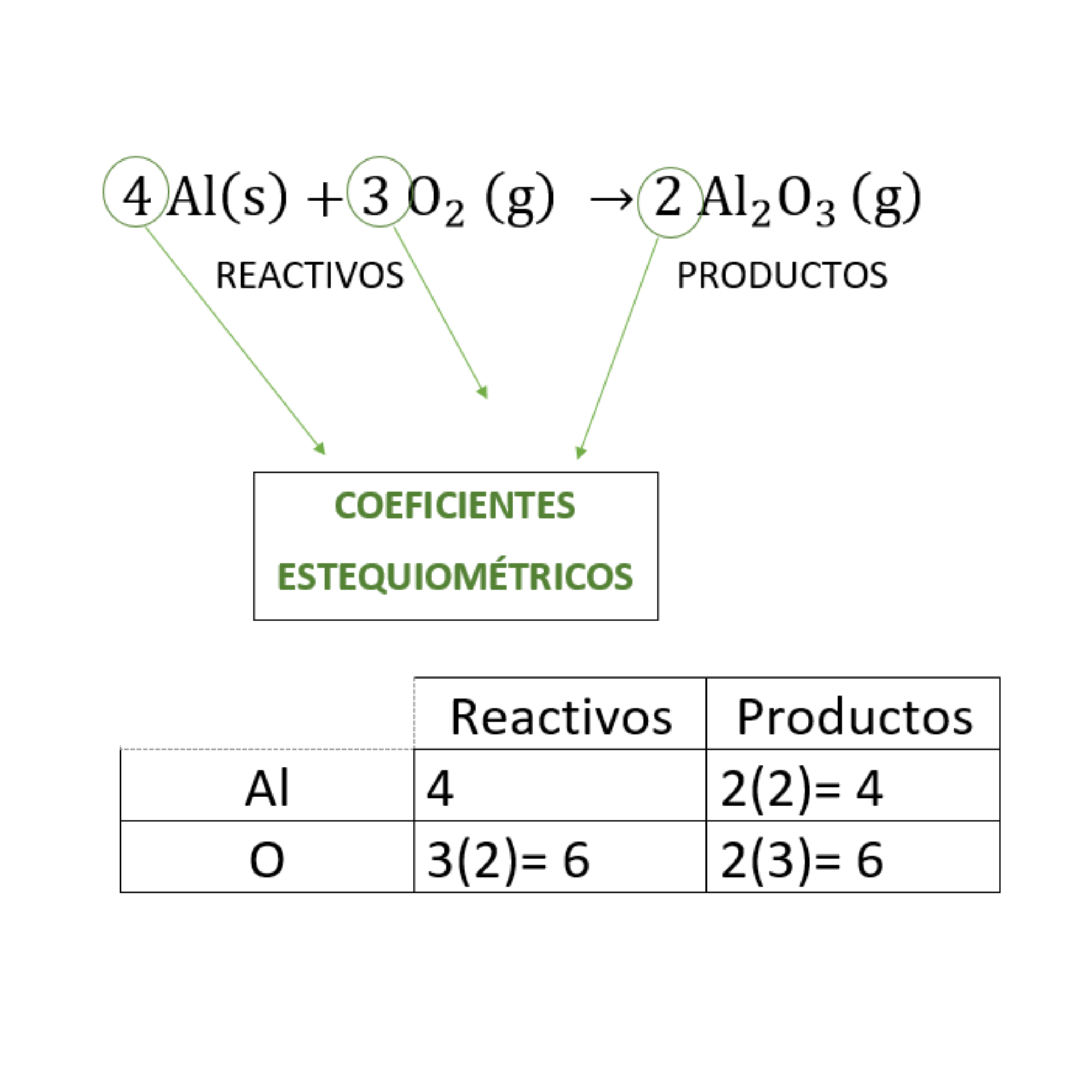
Coeficientes estequiométricosLos
coeficientes estequiométricos indican las cantidades de las
sustancias
químicas
que participan en una reacción química. Los coeficientes estequiométricos son los números escritos adelante de cada fórmula química en las ecuaciones químicas. El balanceo o igualación de ecuaciones químicas se realiza colocando los coeficientes estequiométricos adecuados en la ecuación química.
 |
Composición QuímicaLa
composición química de una sustancia
es
el tipo y cantidad de cada elemento
dentro
de la sustancia. Por ejemplo, la sustancia agua está compuesta por los elementos hidrógeno y oxígeno. En cada molécula de agua, por cada átomo de oxígeno (O) hay 2 átomos de hidrógeno (H). Si se modifica la composición química de una sustancia se transforma en una nueva sustancia.
|
CompuestoUn
compuesto es una sustancia
formada
por dos o más elementos Un ejemplo de compuesto es el agua (H2O), que está compuesta por los elementos químicos hidrógeno y oxígeno. |
D |
|---|
DipoloUn dipolo es un sistema formado por dos cargas opuestas (una de las cargas es positiva y la otra carga es negativa). Las cargas se encuentran cercanas. En una molécula se forma un dipolo cuando una región de la molécula tiene carga parcial positiva y otra región de la molécula tiene carga parcial negativa. |
Disolución o Solución |
Disolvente o Solvente |
E |
|---|
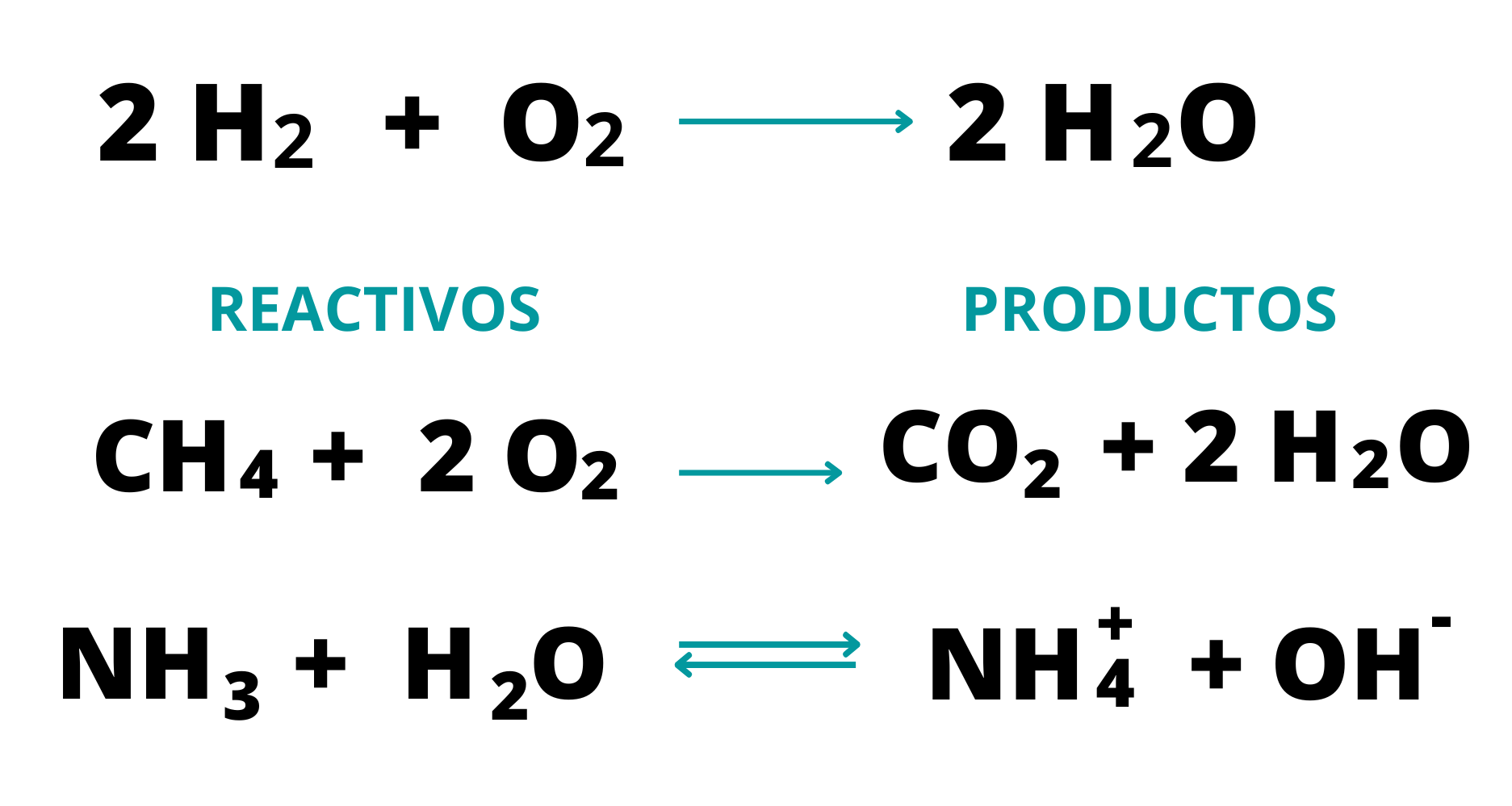
Ecuación QuímicaLa ecuación química es la representación de una reacción química. En
las ecuaciones químicas se usan las fórmulas
químicas
de
los
reactivos
y
productos Las ecuaciones químicas están balanceadas cuando la cantidad de átomos de cada elemento en los reactivos es igual a la cantidad de átomos de cada elemento en los productos Es frecuente que en las ecuaciones químicas se muestre el estado de agregación de cada sustancia.
 |
Electrón |
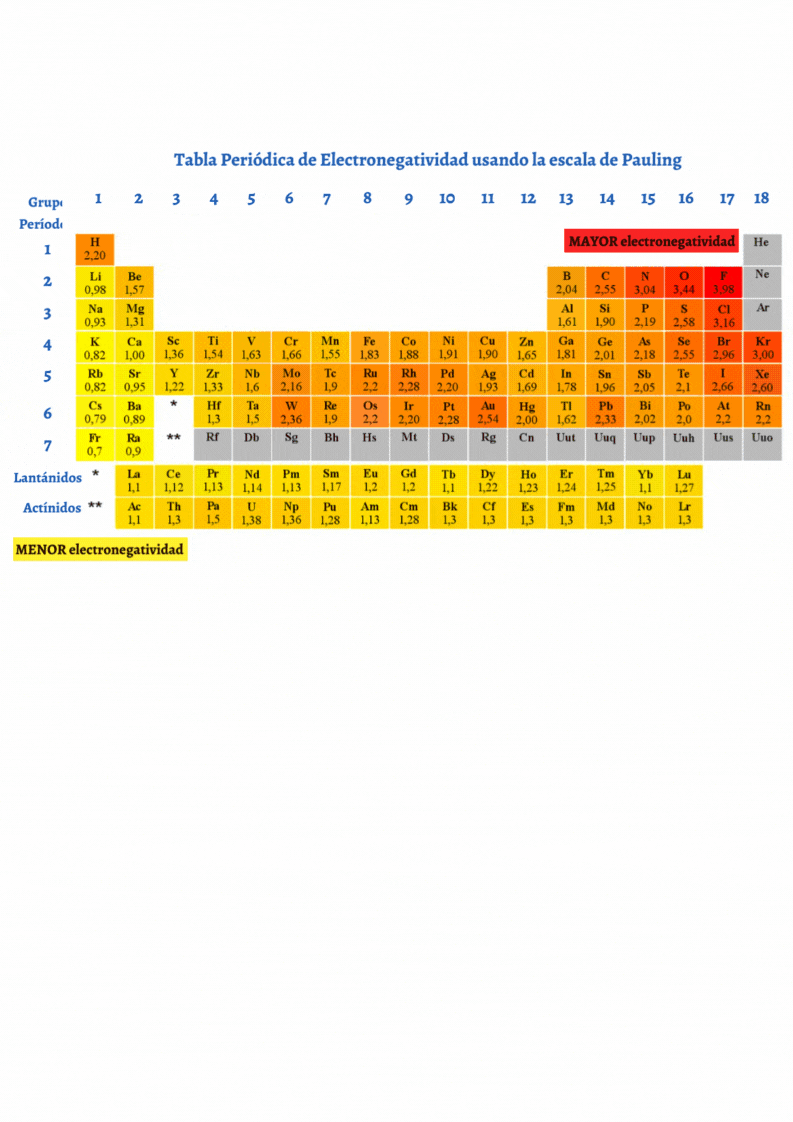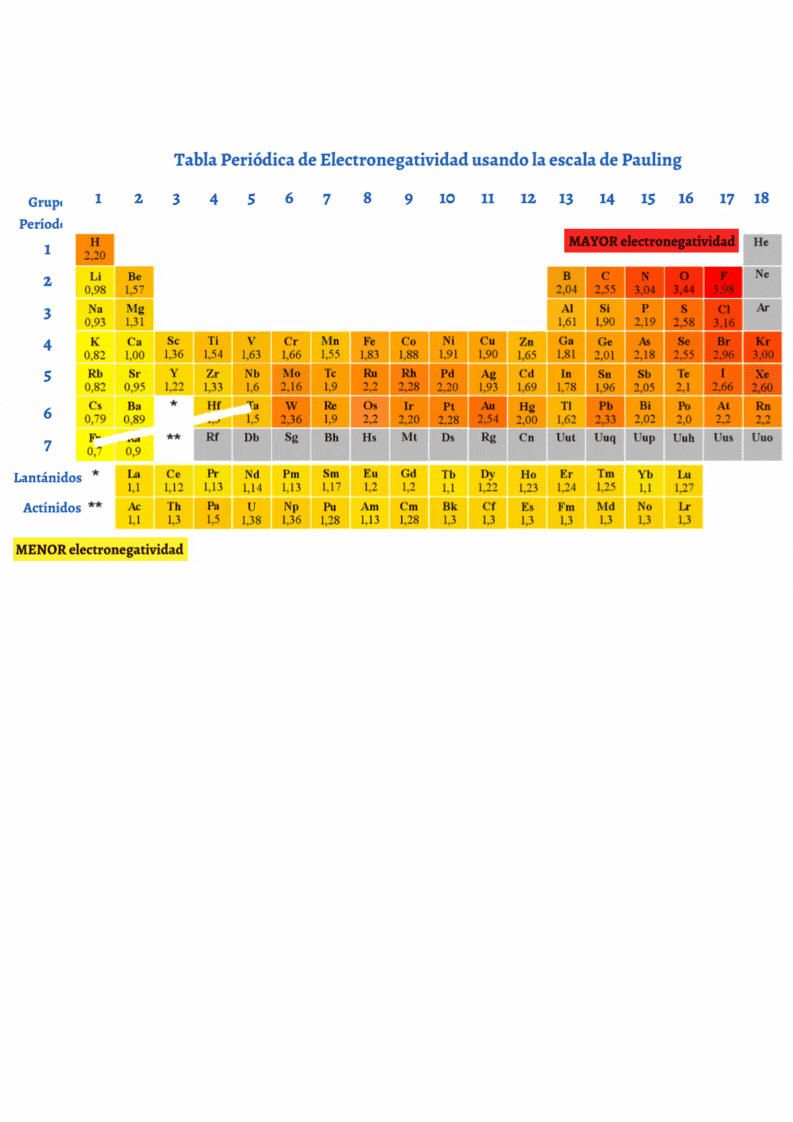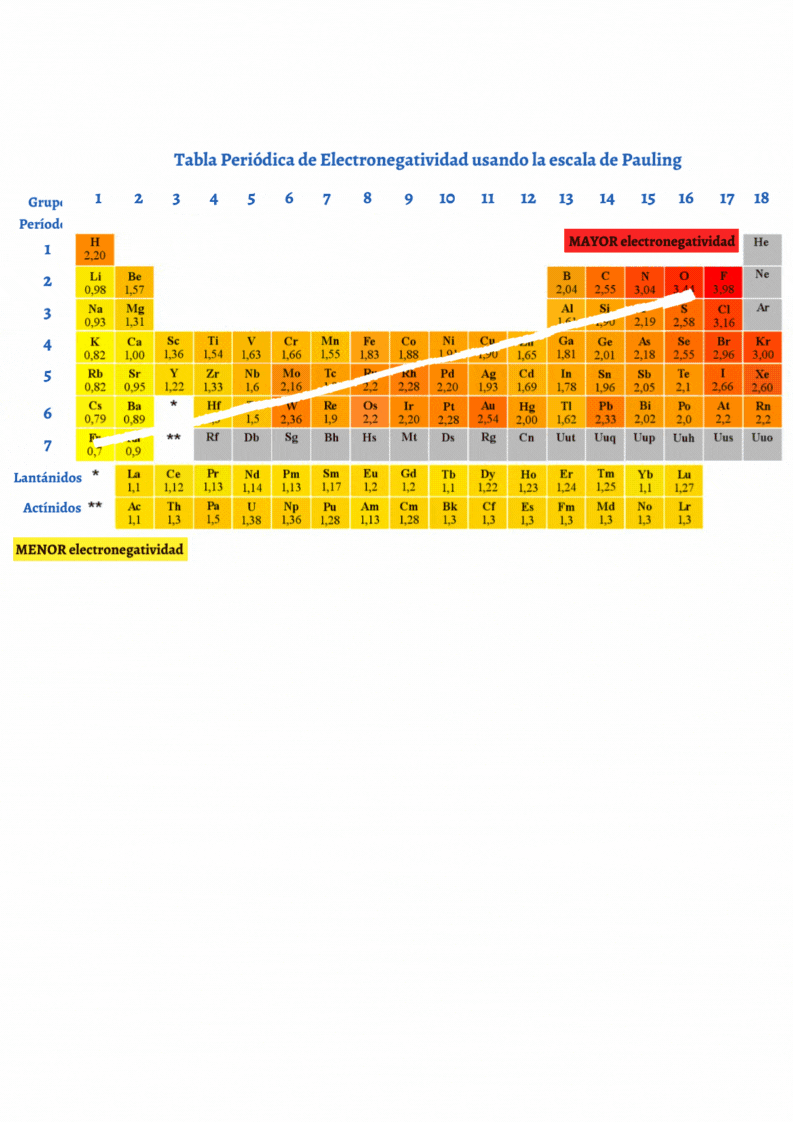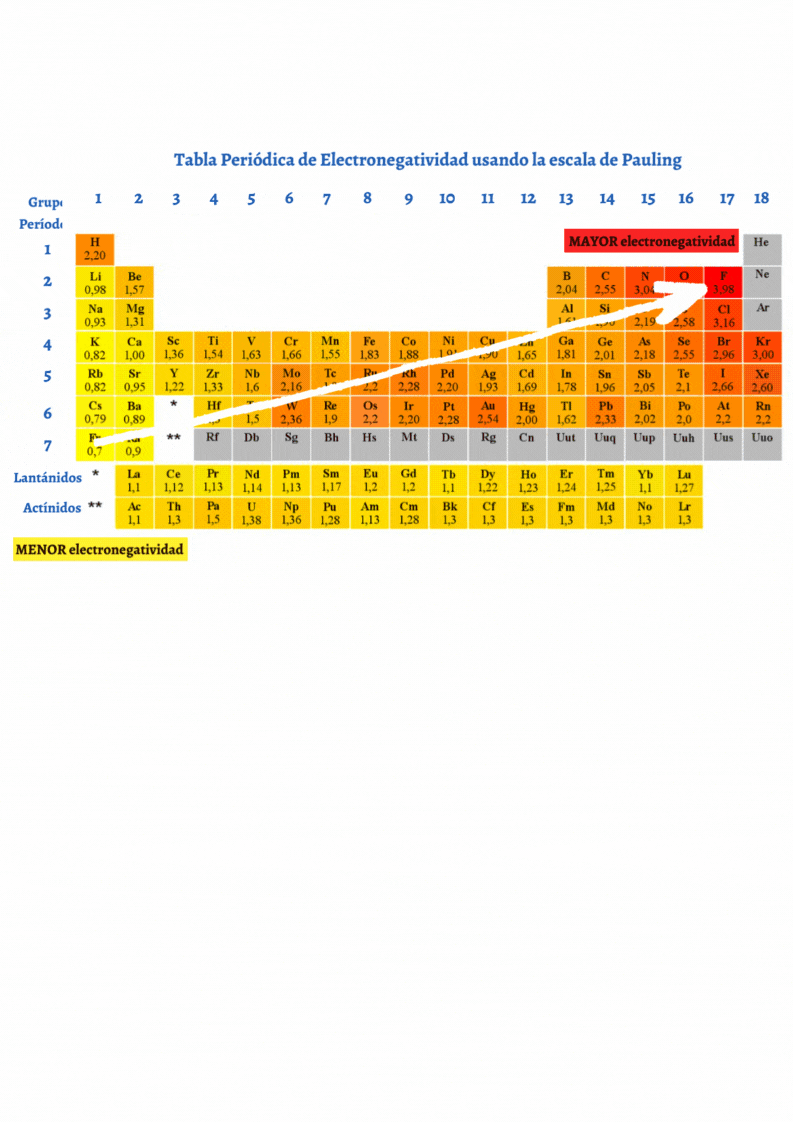
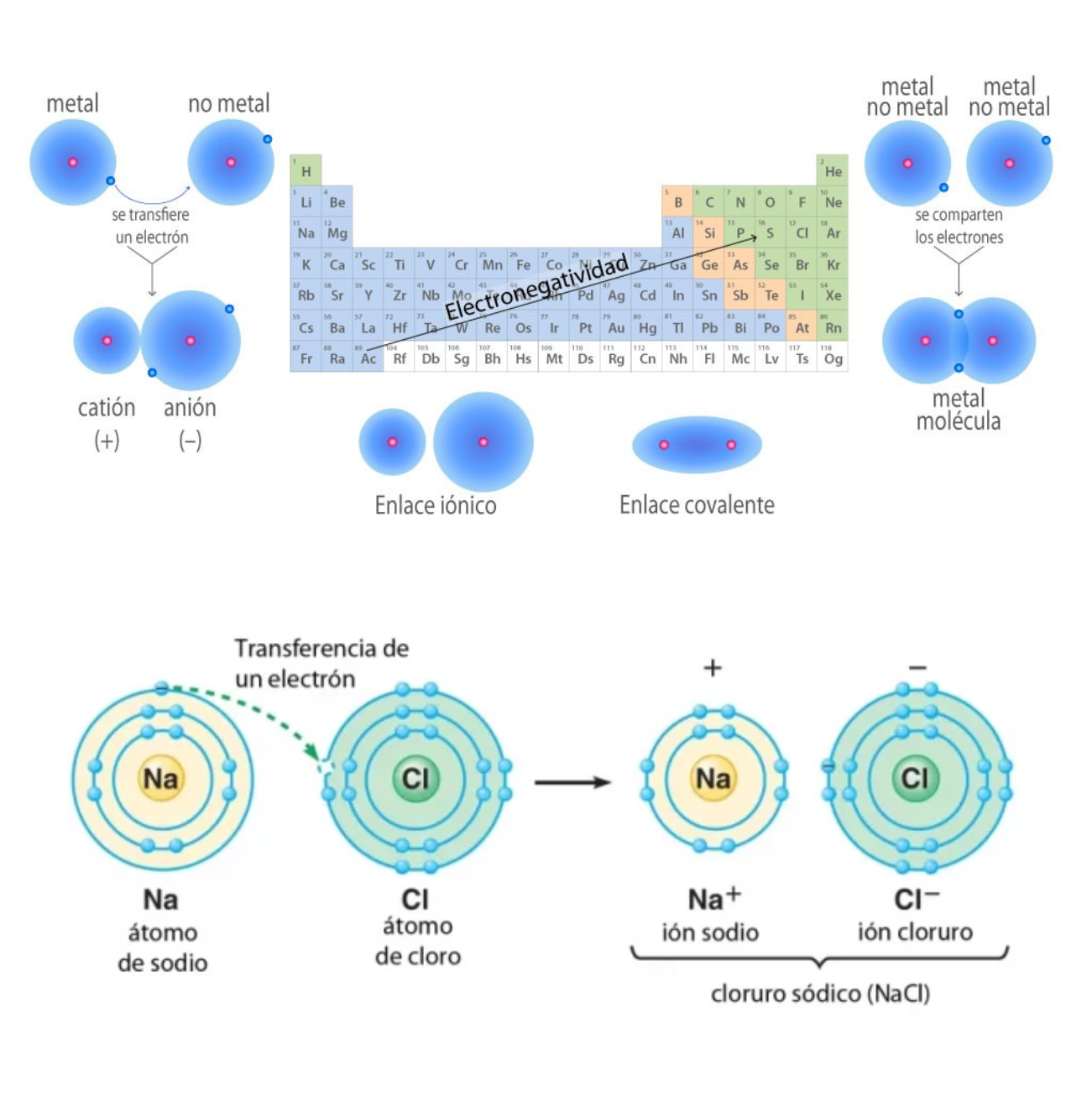
ElectronegatividadLa electronegatividad es la capacidad de un átomo que está unido a otro átomo de atraer electrones del enlace. Cuanto mayor sea la electronegatividad, la capacidad de atraer los electrones del enlace será mayor. La diferencia entre las electronegatividades de los átomos en un enlace determina el tipo de enlace químico.
|
Elemento QuímicoEl elemento químico es una sustancia que no se puede descomponer en otra sustancia más simple. Cada elemento químico se representa con un símbolo químico formado por una letra o por dos letras. Por ejemplo, el elemento nitrógeno se representa como N, y el elemento calcio como Ca. Todos los elementos conocidos se ordenan en la Tabla Periódica. Todos los átomos de un mismo elemento tienen la misma cantidad de protones.
 |
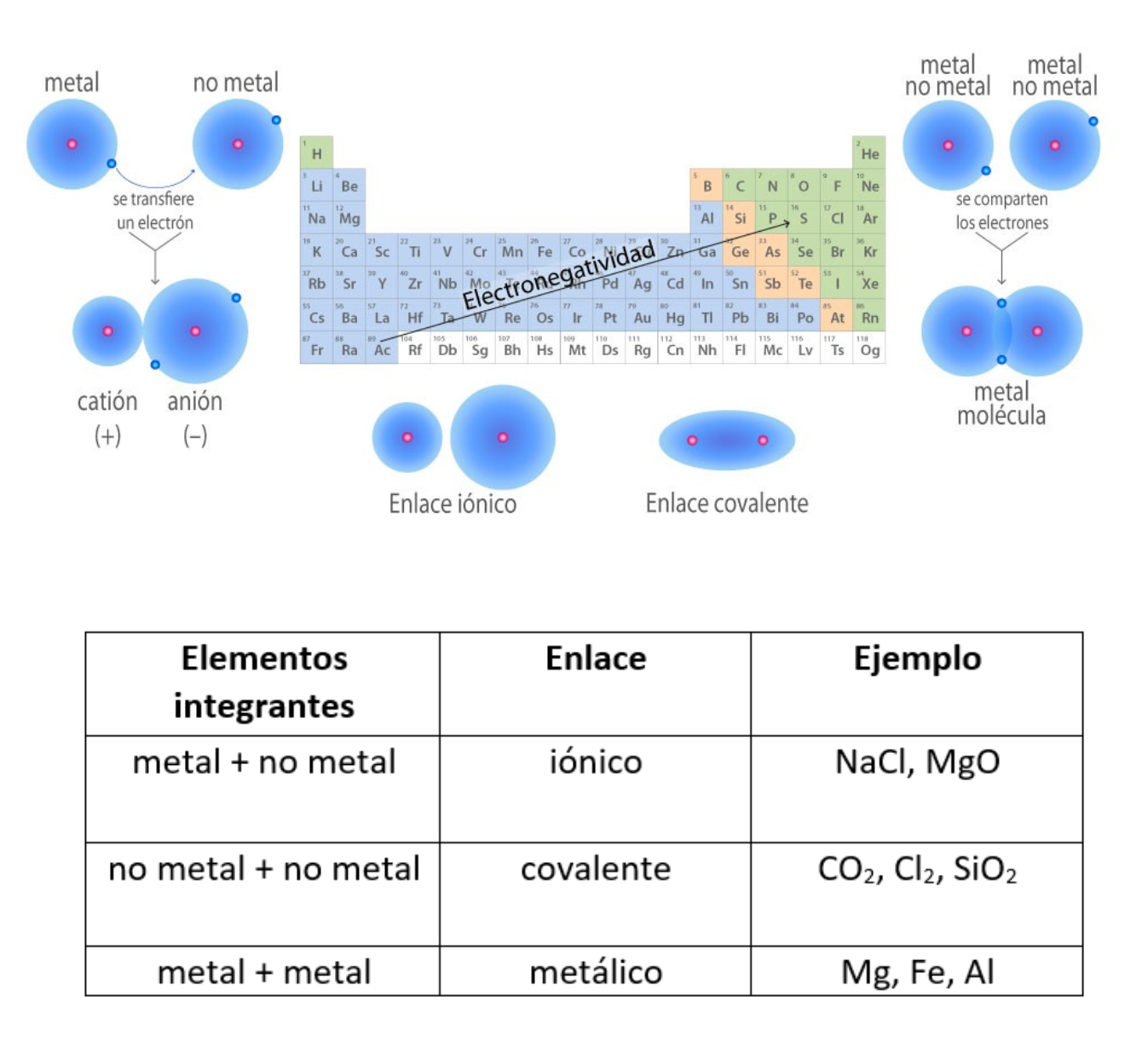
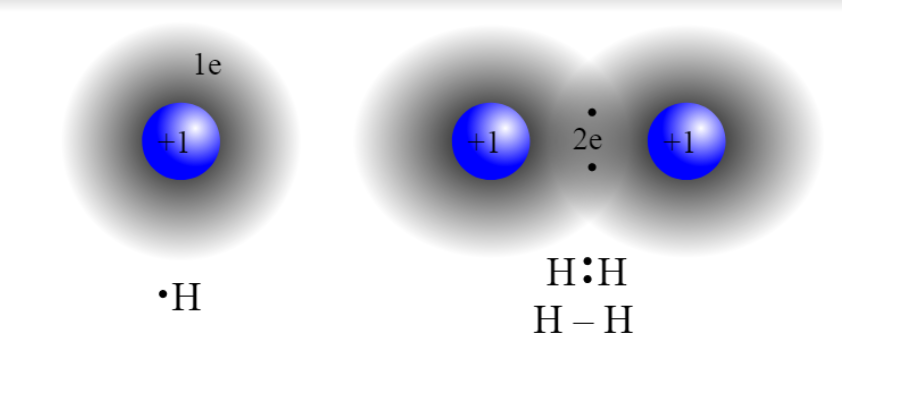
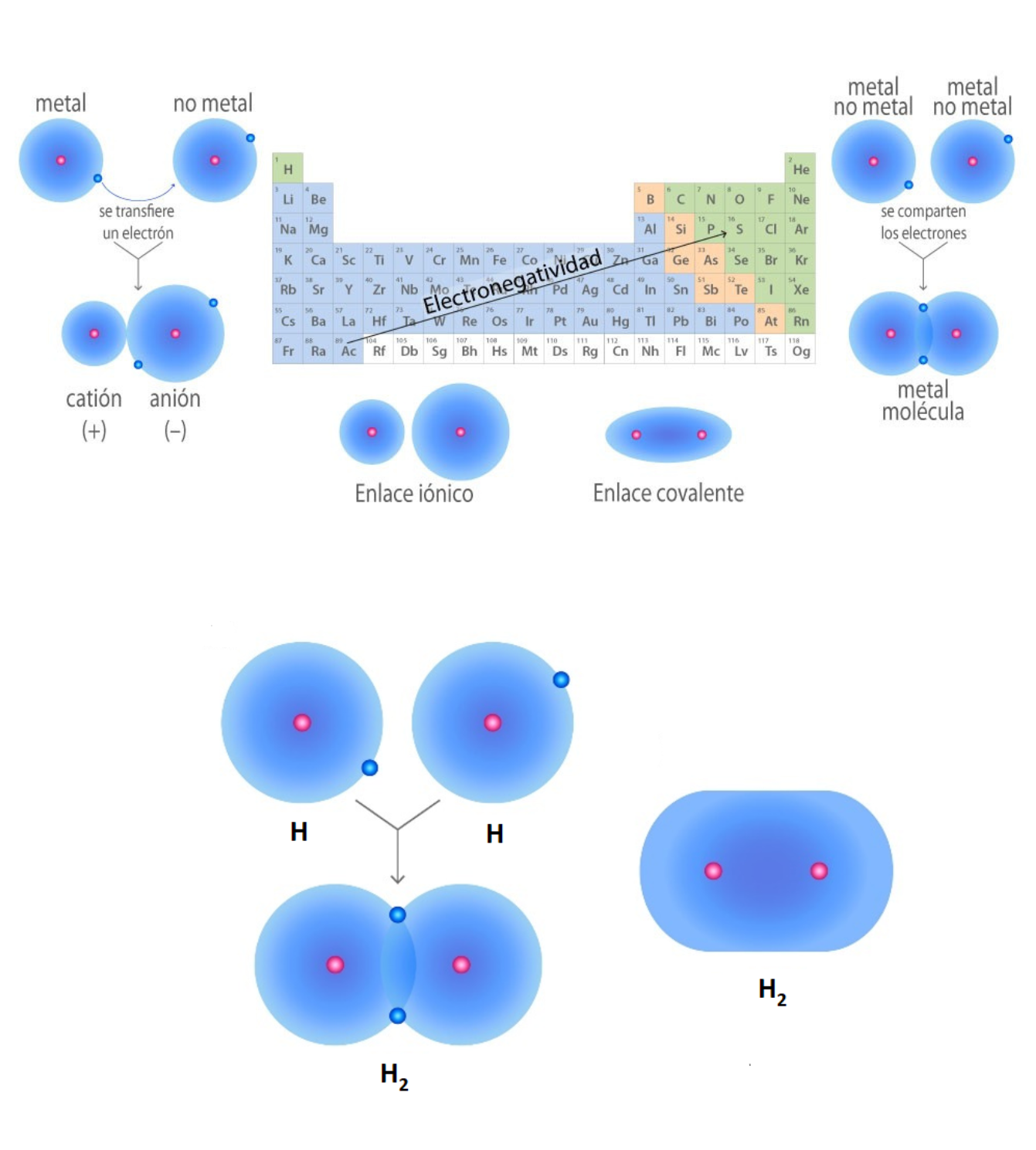
Enlace CovalenteEl
enlace covalente es un enlace
químico
formado
entre dos átomos
que
comparten electrones. La diferencia de electronegatividad entre los átomos que se enlazan puede ser de nula a intermedia. Se llama enlace covalente no polar cuando los electrones del enlace se comparten por igual entre los átomos. En este caso la diferencia de electronegatividad es nula. Se llama enlace covalente polar cuando los electrones del enlace no se comparten por igual entre los átomos. En este caso la diferencia de electronegatividad es intermedia.
 |
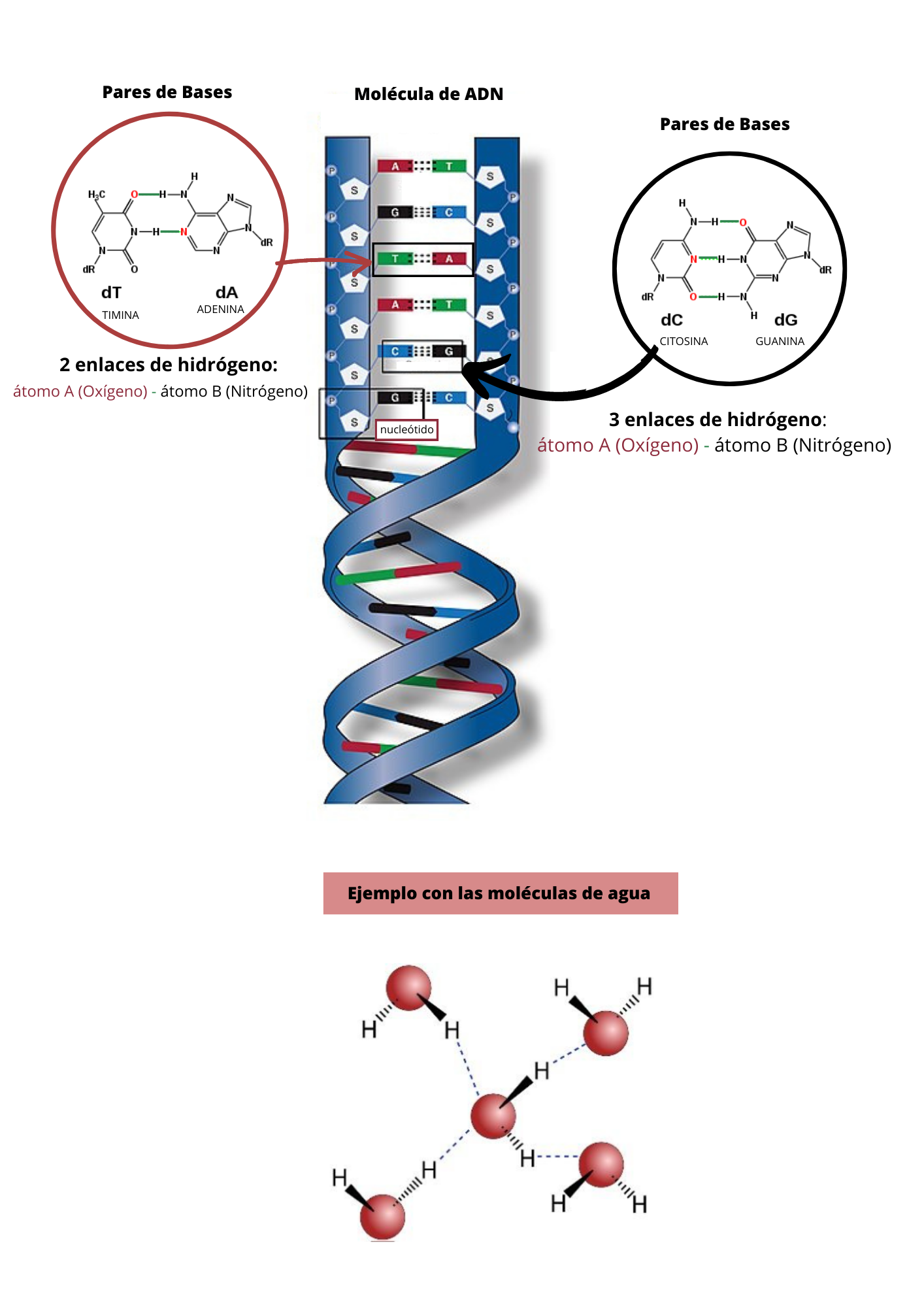
Enlace de hidrógeno
Enlace de Hidrógeno El enlace de hidrógeno es un tipo de enlace de baja energía. El enlace de hidrógeno se establece entre un átomo de hidrógeno y un átomo electronegativo A. Para que se forme el enlace de hidrógeno, el átomo de hidrógeno debe estar unido por enlace covalente a un átomo electronegativo B. El Enlace de Hidrógeno antes se llamaba Puente de Hidrógeno. Por lo general A y B, son oxígeno (O), nitrógeno (N), flúor (F) o cloro (Cl).
|
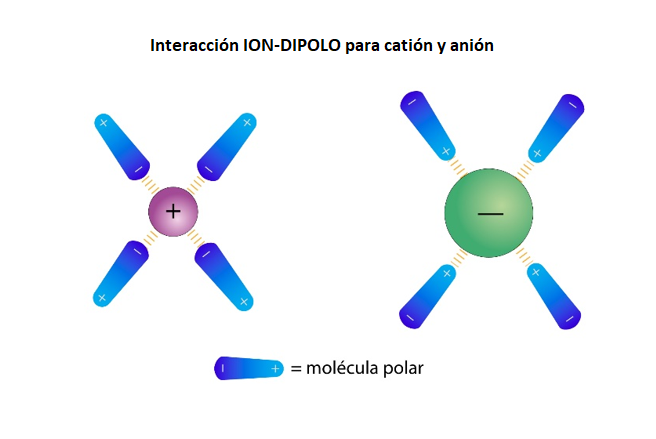
Enlace Ion-Dipolo |
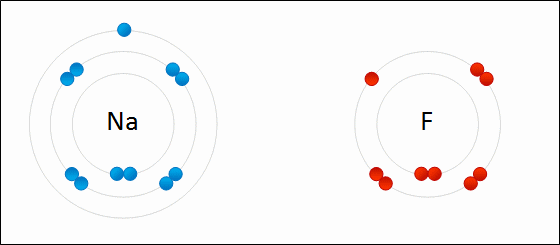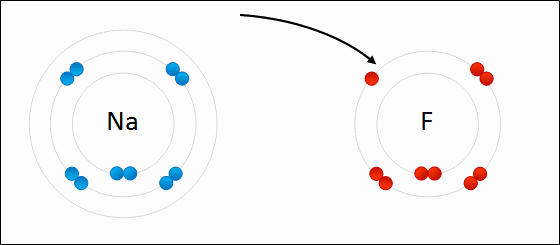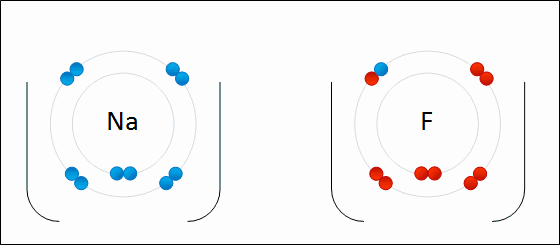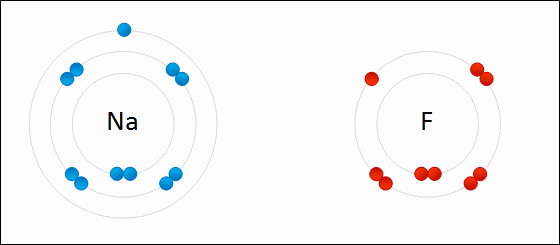
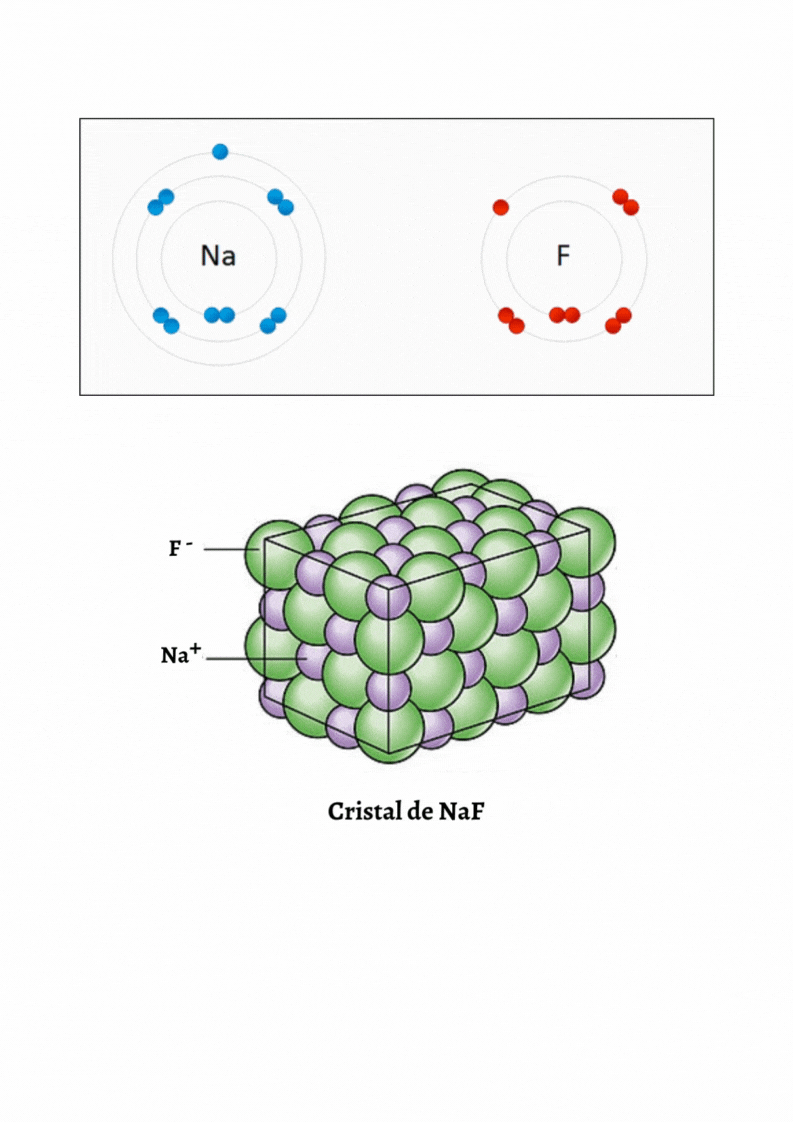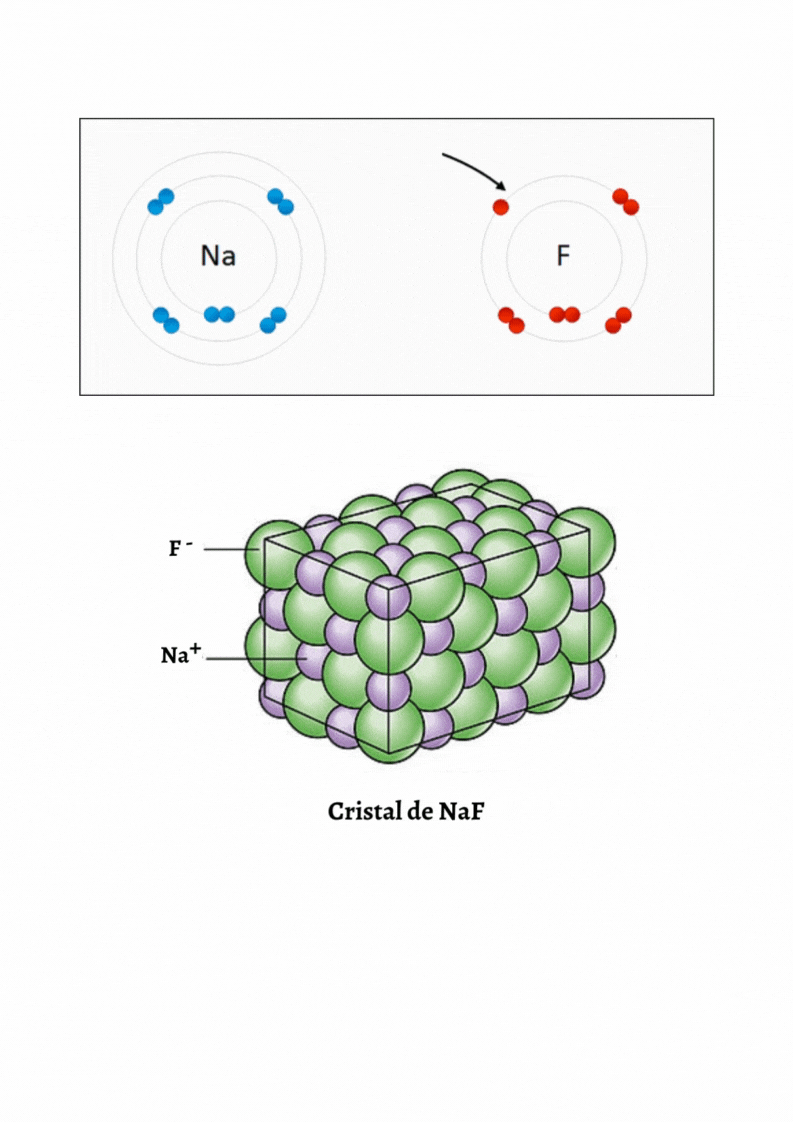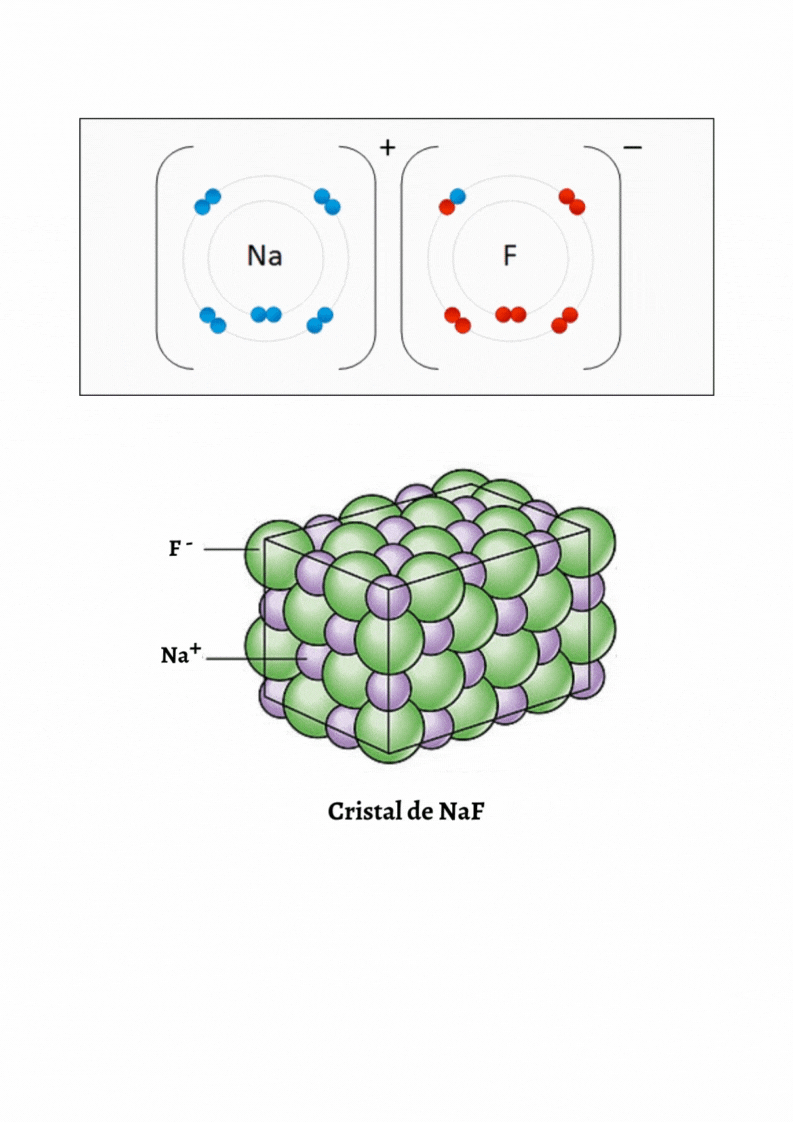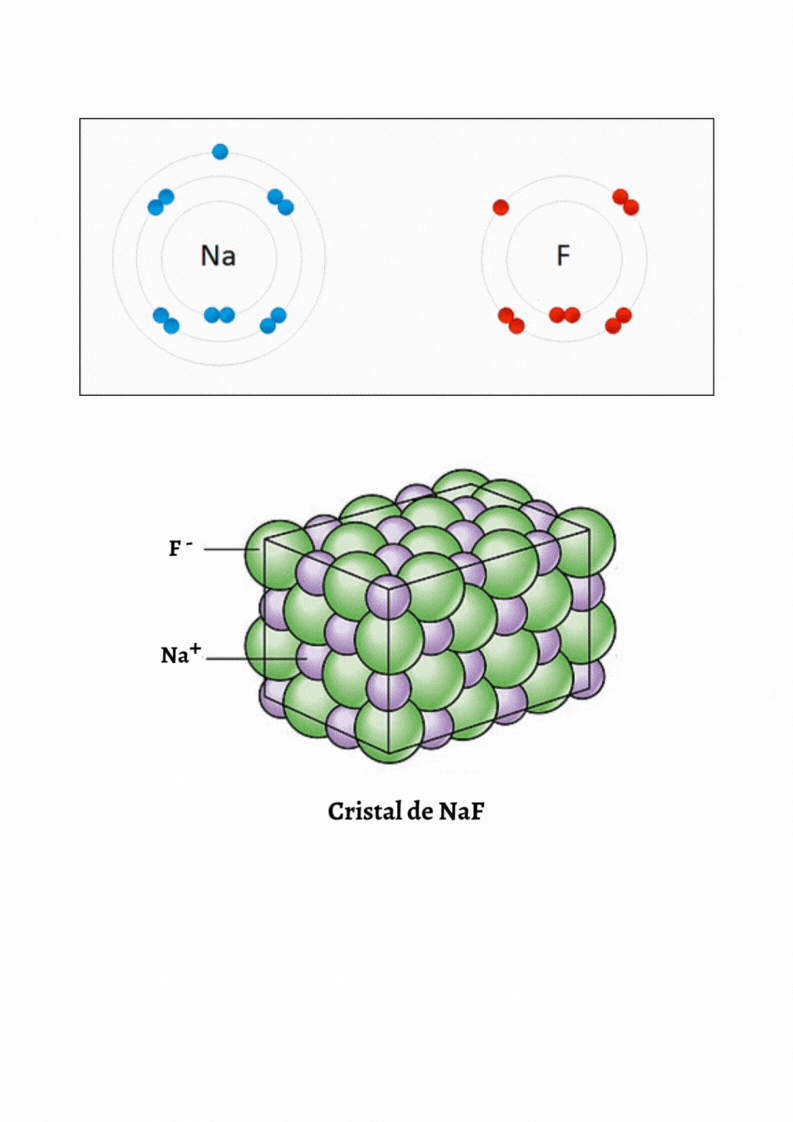
Enlace IónicoEl
enlace iónico es el enlace que mantiene unido a los cationes y
aniones en las sustancias
iónicas. Un enlace iónico es la atracción electrostática entre las cargas eléctricas de cationes y aniones. Los cationes y aniones se forman a partir de átomos con una diferencia de electronegatividad muy grande.
|
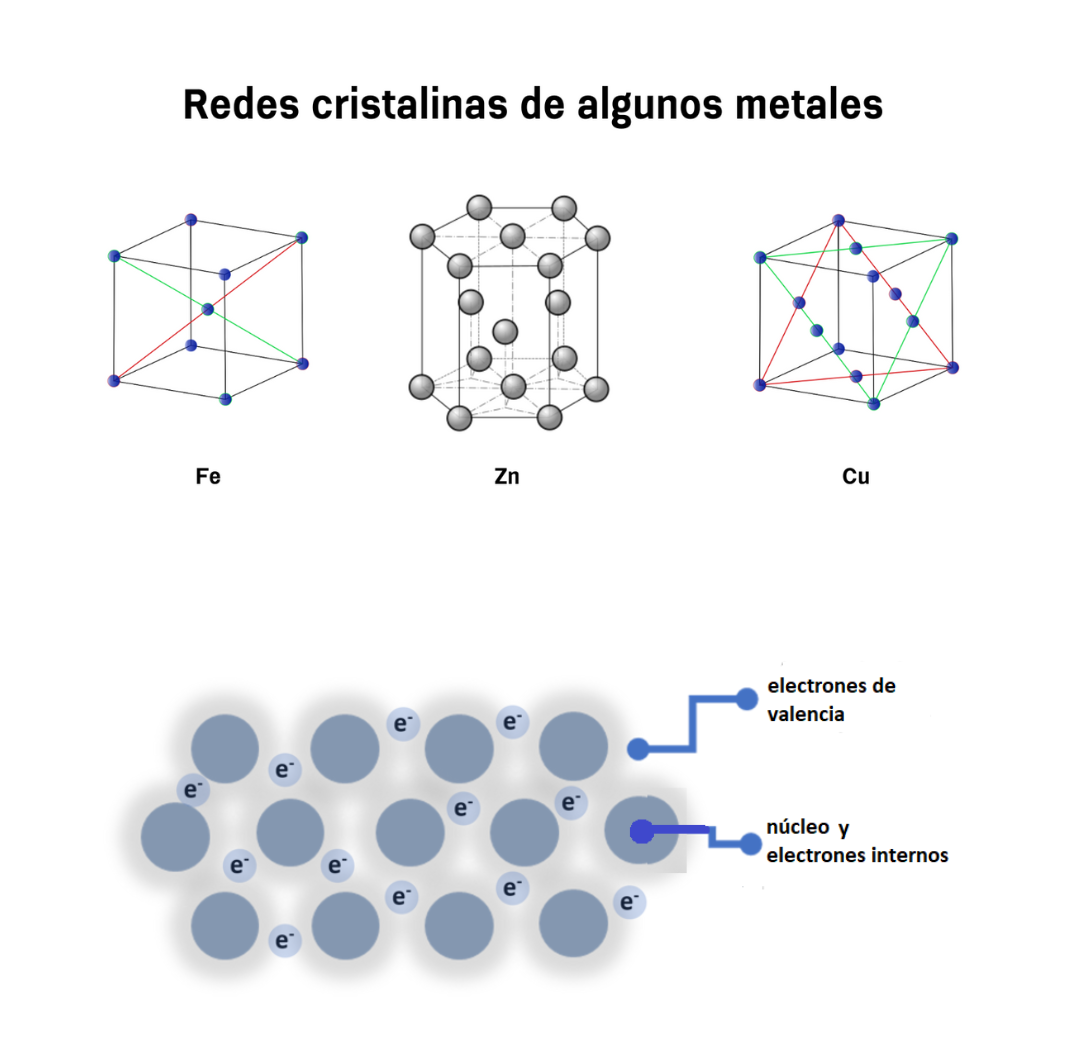
Enlace MetálicoEl enlace metálico es un enlace químico que mantiene unidos a los átomos de los metales. En el enlace metálico los núcleos y los electrones internos de los átomos se encuentran ordenados en una red cristalina. Los electrones de valencia de esos átomos se mueven de forma libre a lo largo de todo el metal. Los electrones de valencia se comparten entre todos los átomos del metal. Los electrones de valencia del metal están deslocalizados. El enlace metálico genera características en los metales. Los metales:
|
Enlace Químico (Unión Química)El
enlace químico es la fuerza que une átomos,
moléculas
o
iones
entre
sí. Los enlaces químicos generan grupos de átomos, moléculas o iones unidos entre sí de forma estable. Por ejemplo, el enlace que existe entre 2 átomos de hidrógeno (H) forma la molécula de dihidrógeno (H2). Tipos de enlaces:
|
Enlaces de Baja EnergíaSon
enlaces
químicos
que
poseen baja energía
de enlace
y
actúan a distancias muy cortas. Los enlaces de baja energía tienen menor energía que los enlaces:
Existen diferentes tipos de enlaces de baja energía:
|
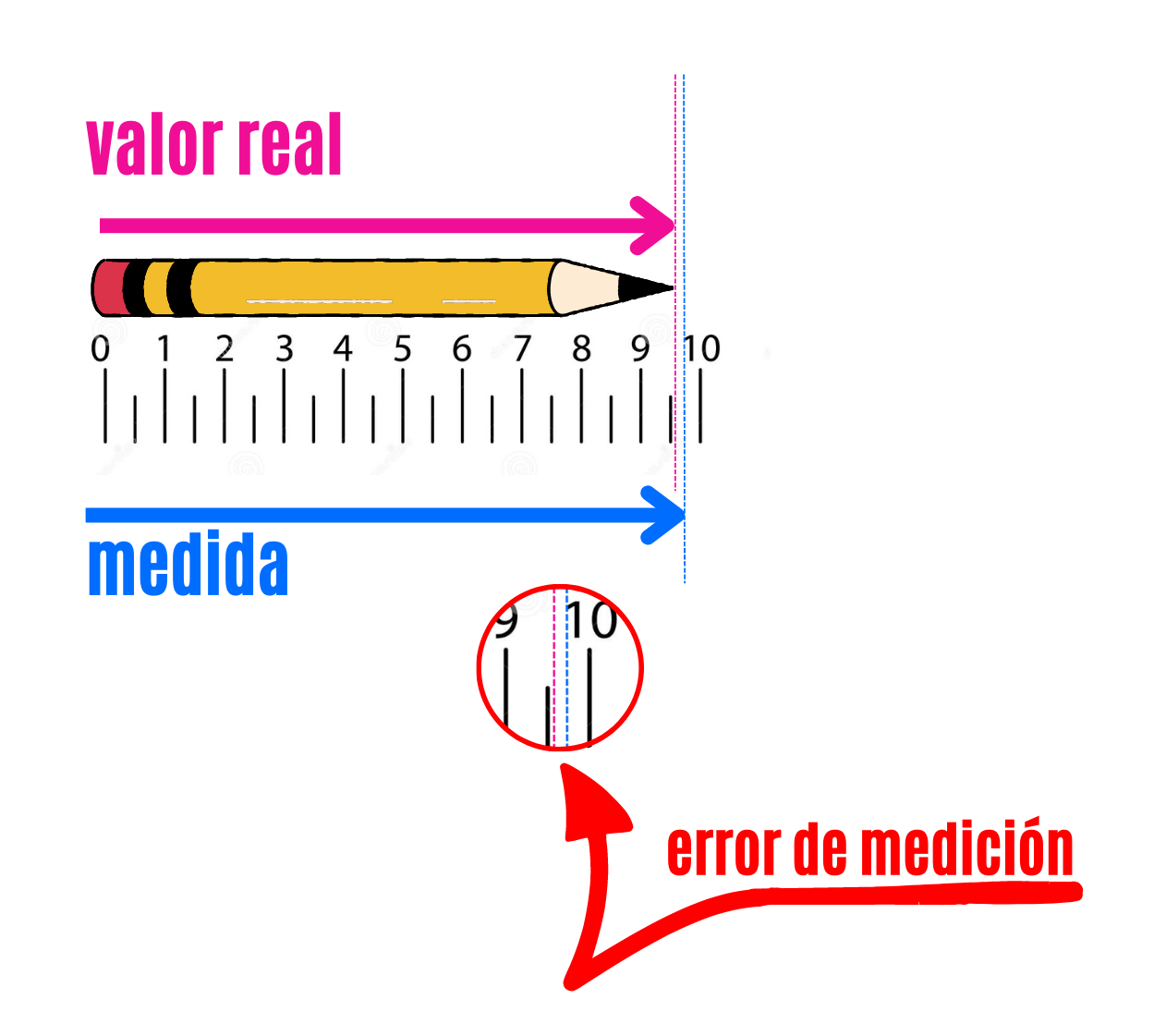
Error de Medición |
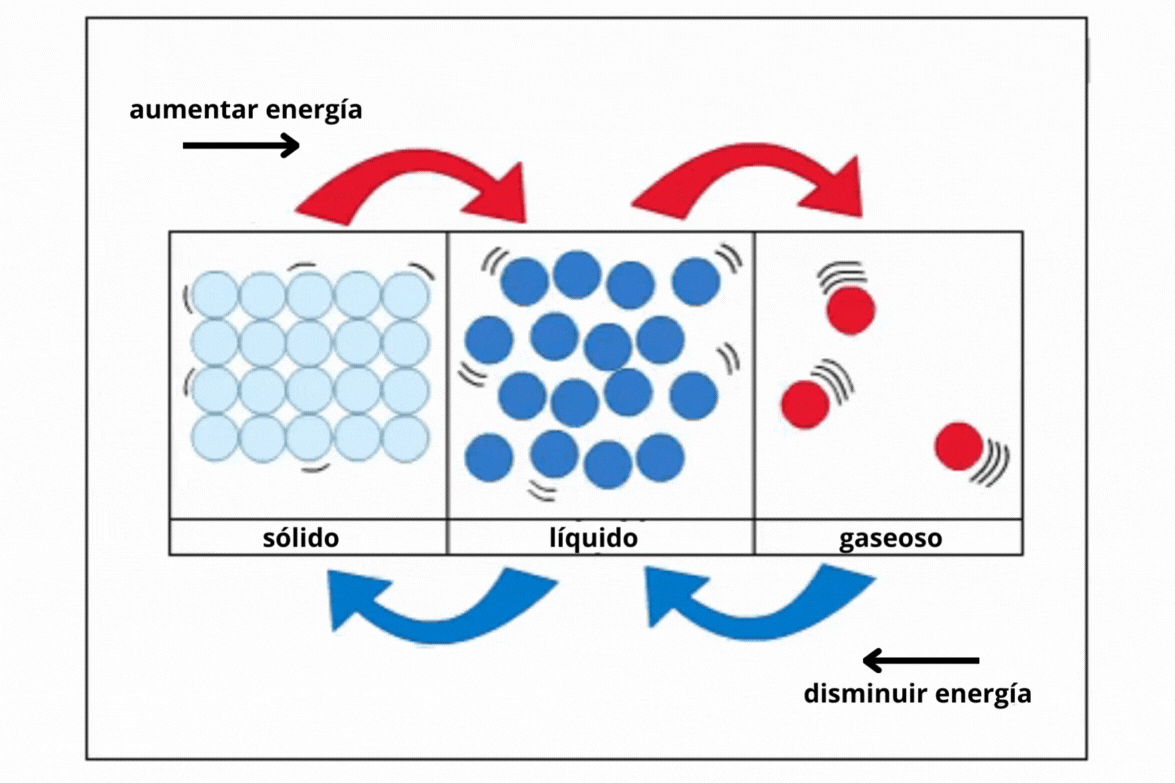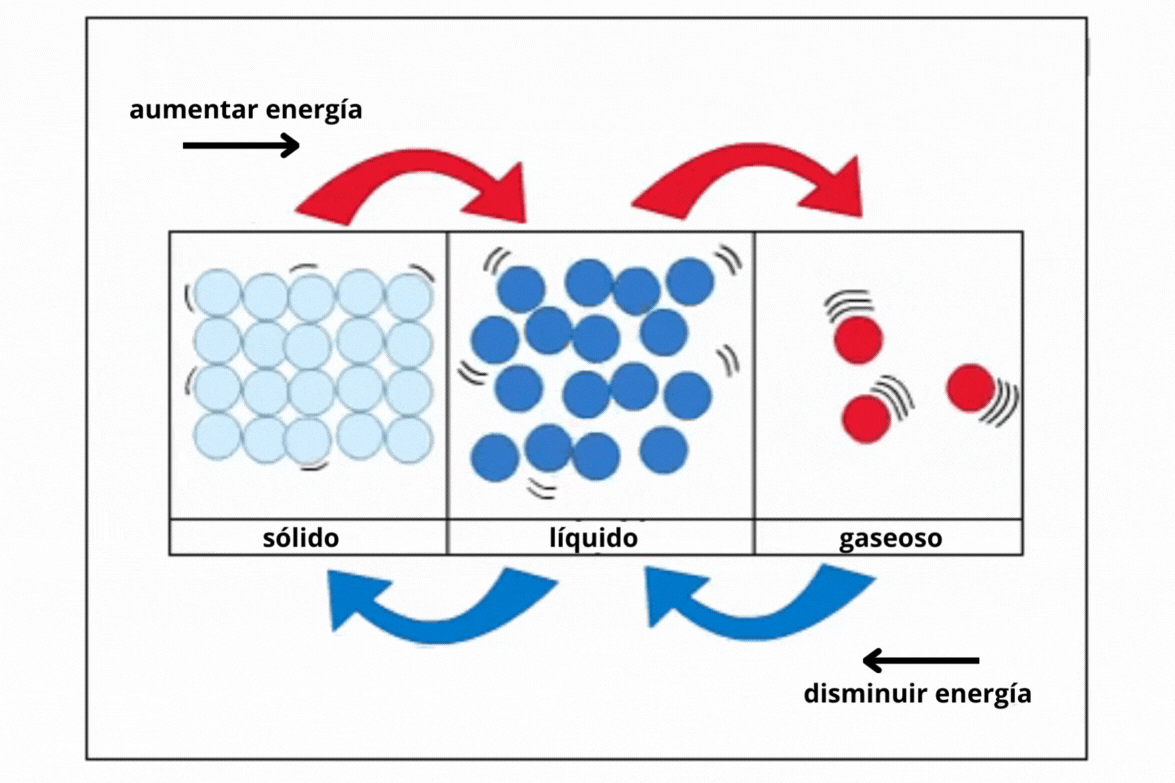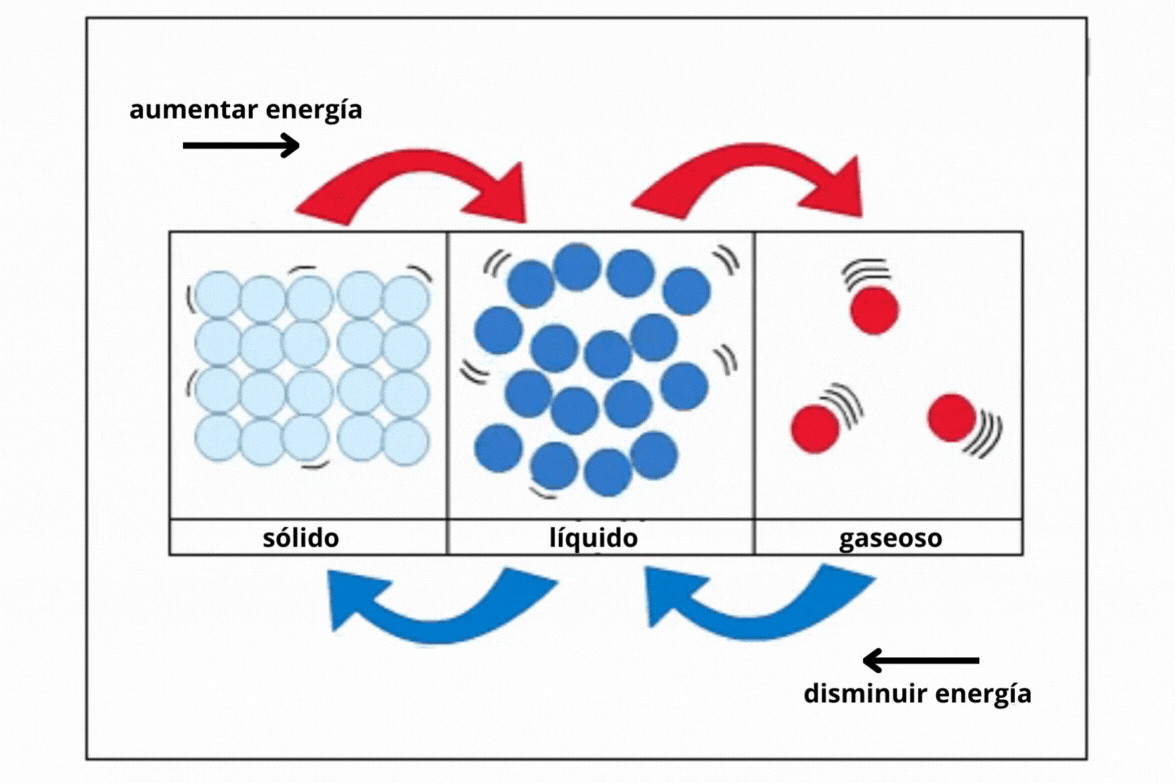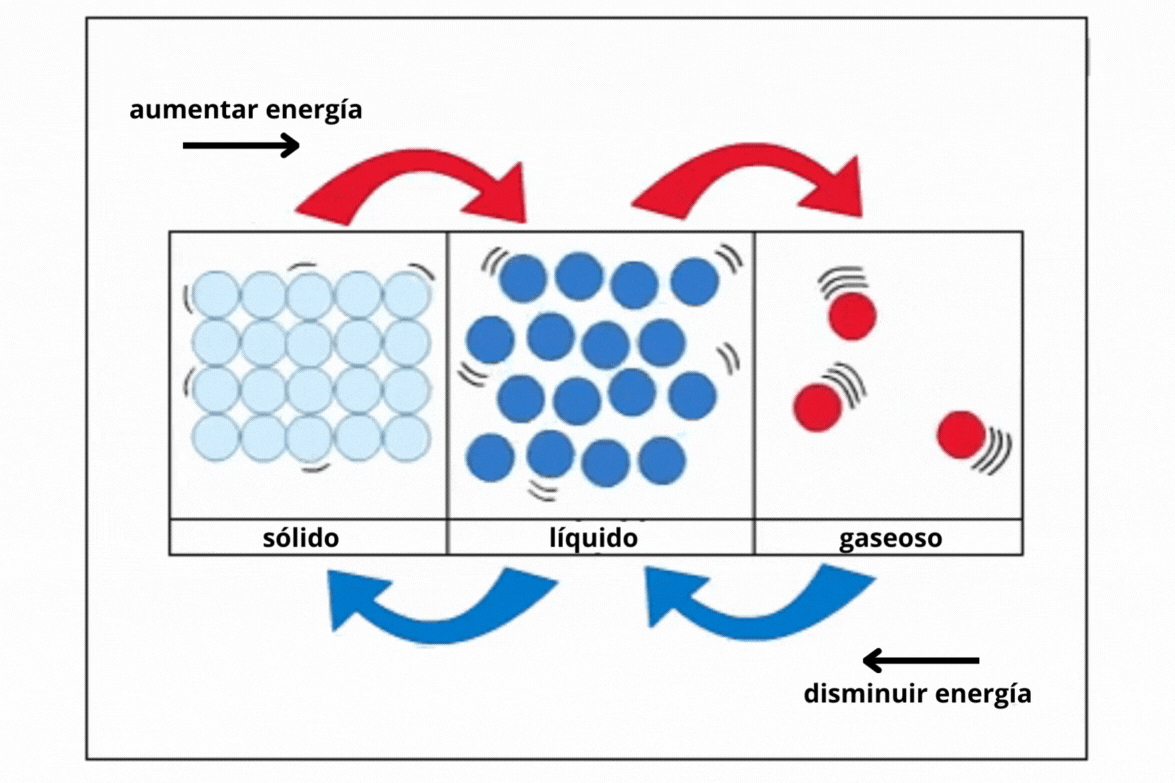
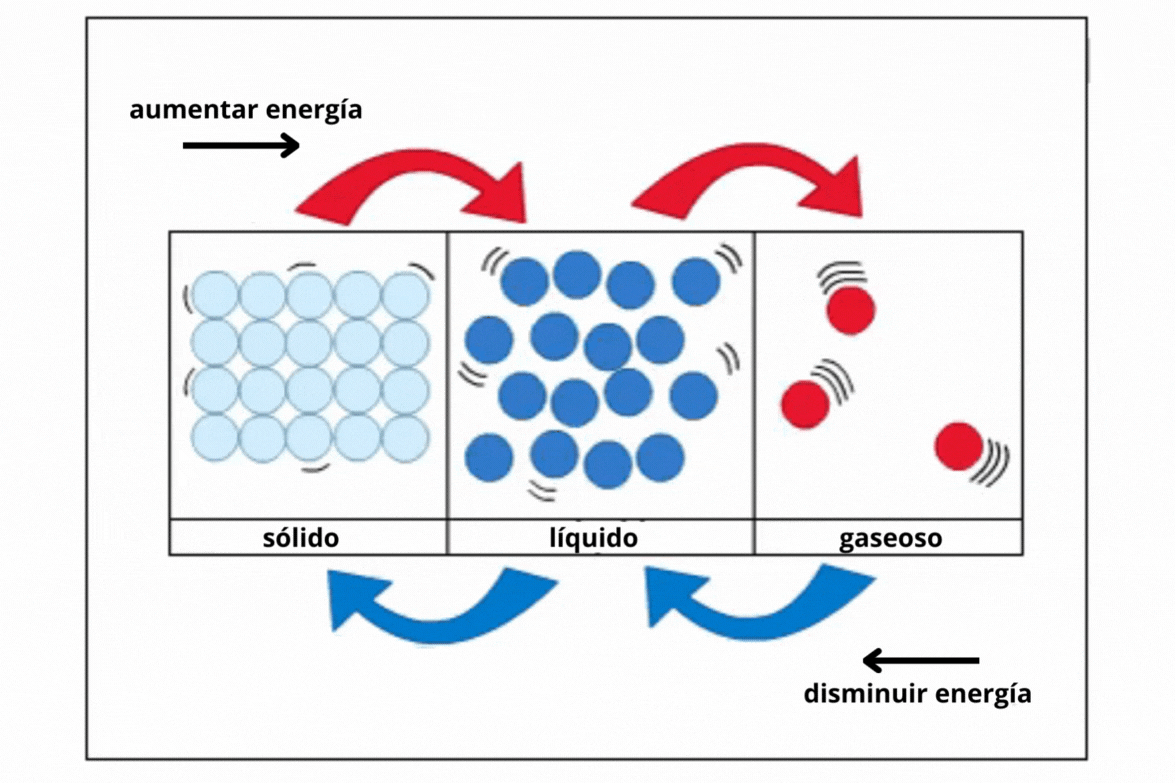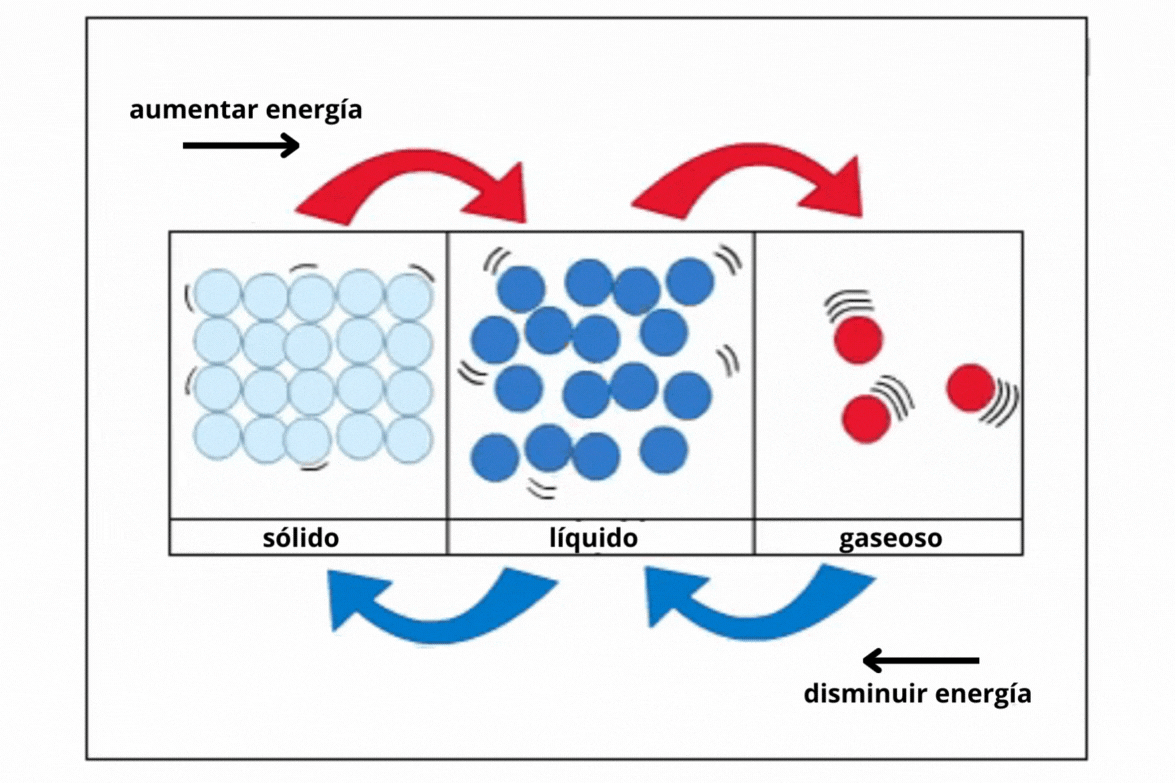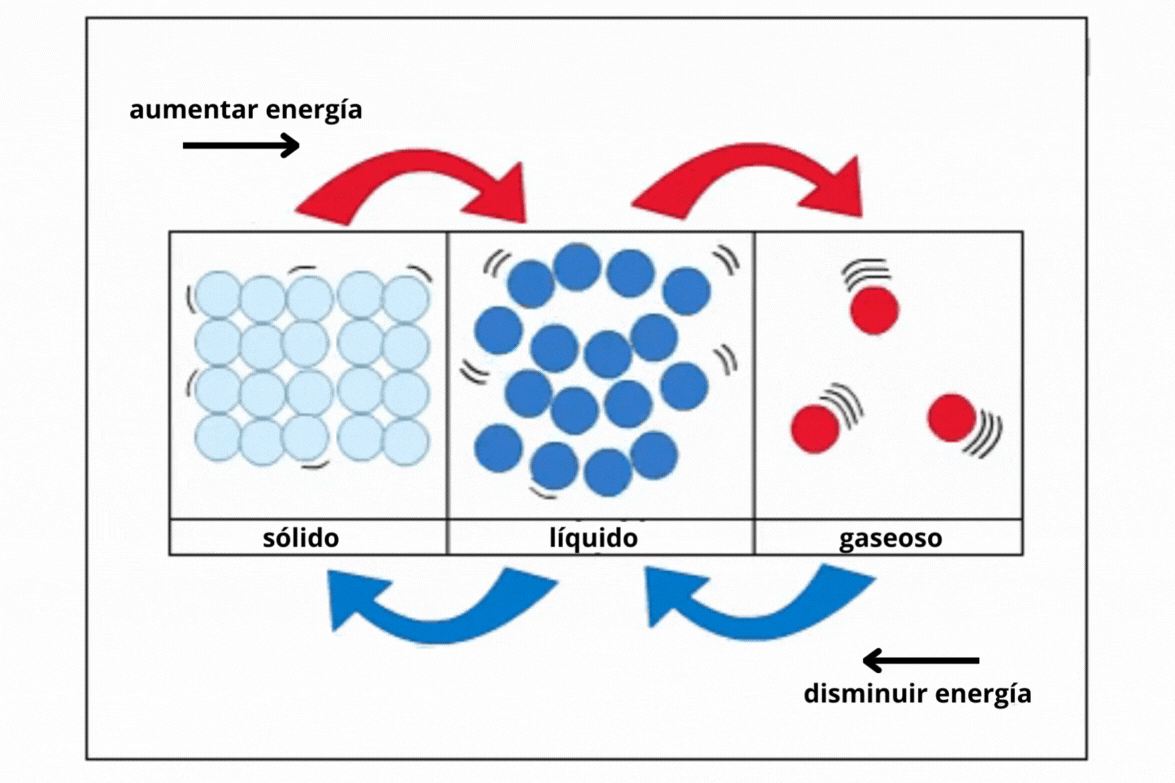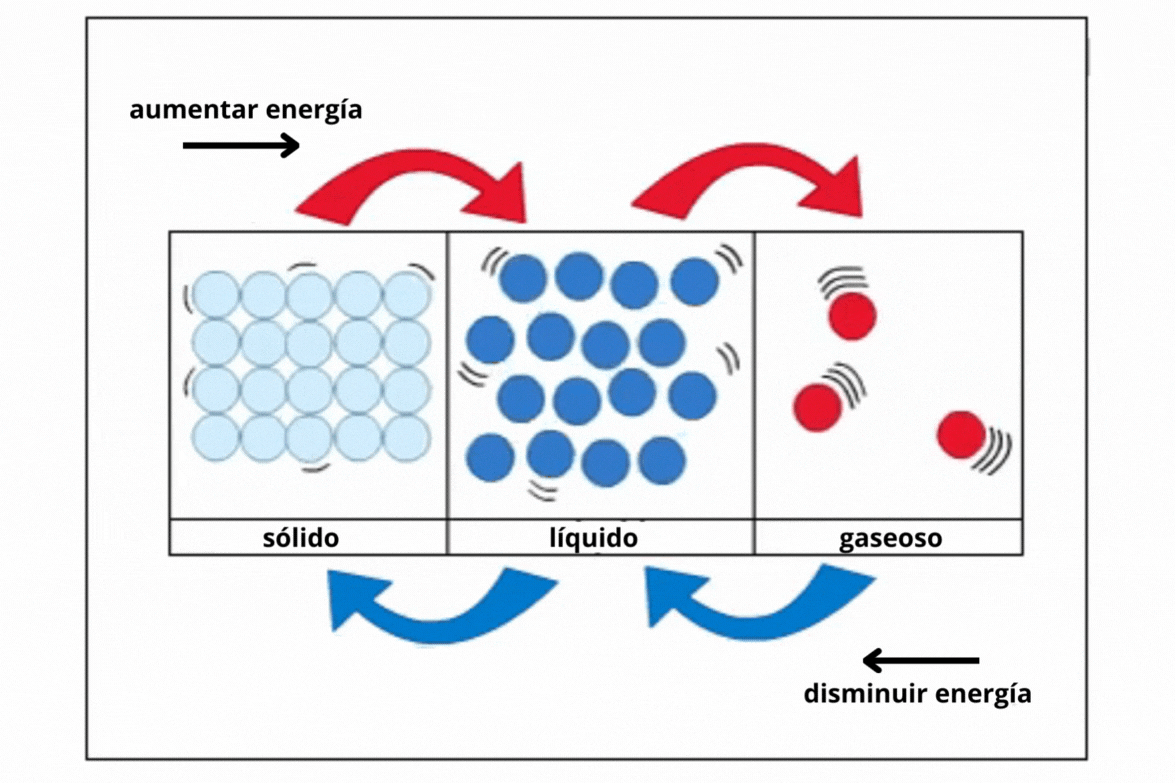
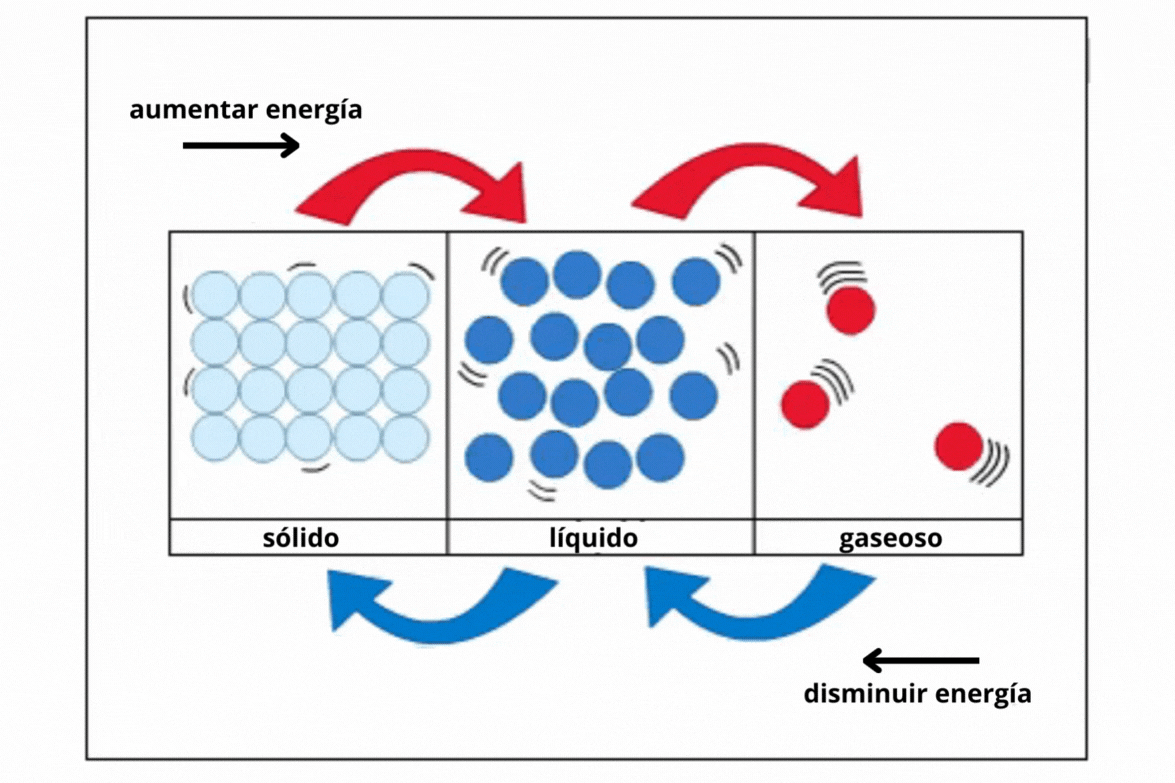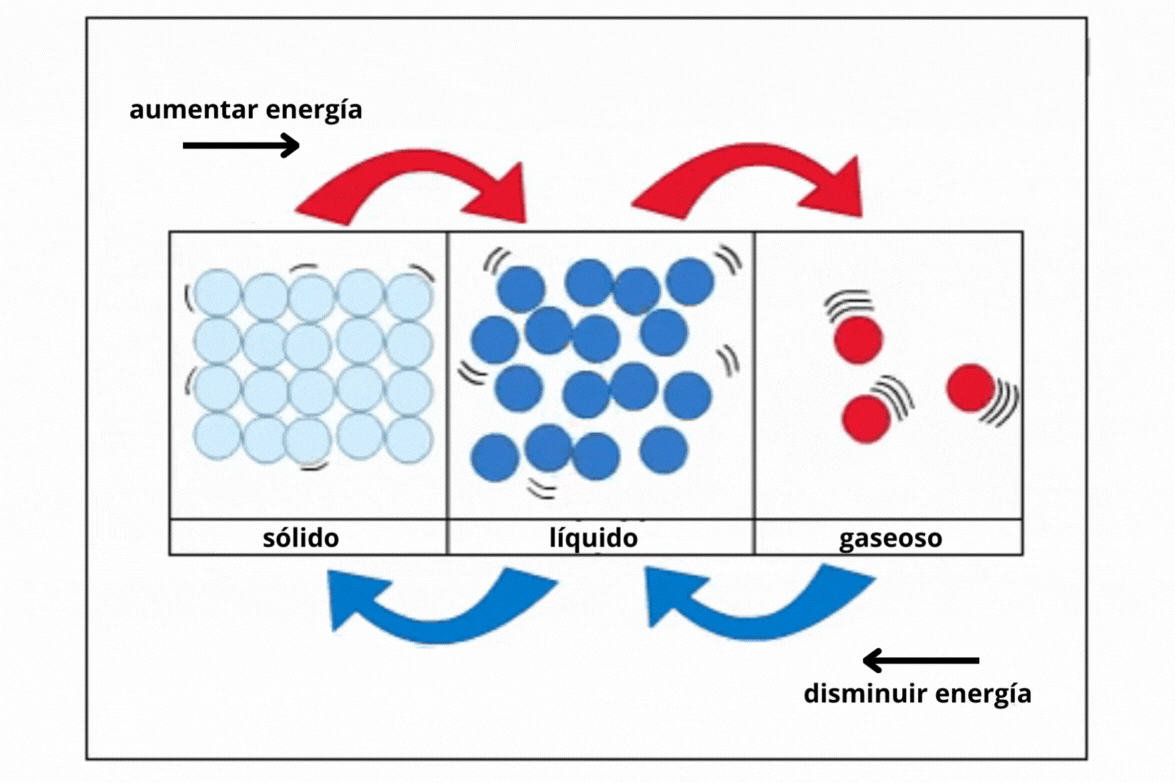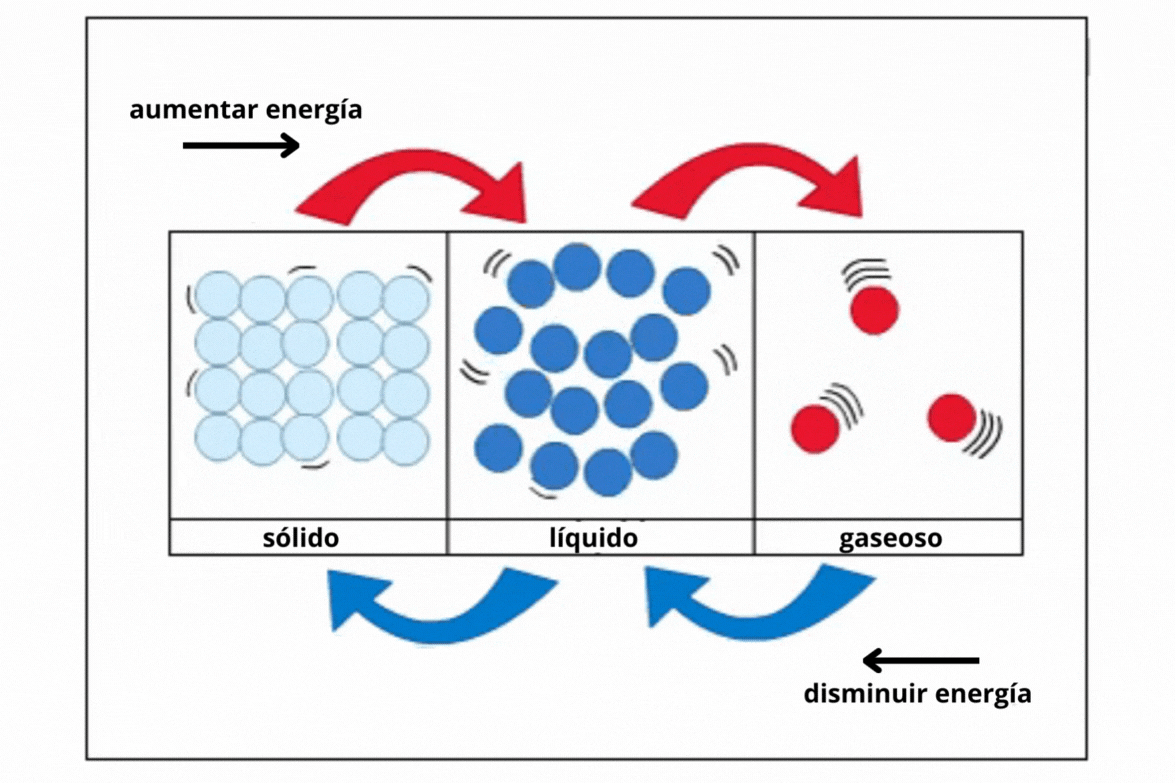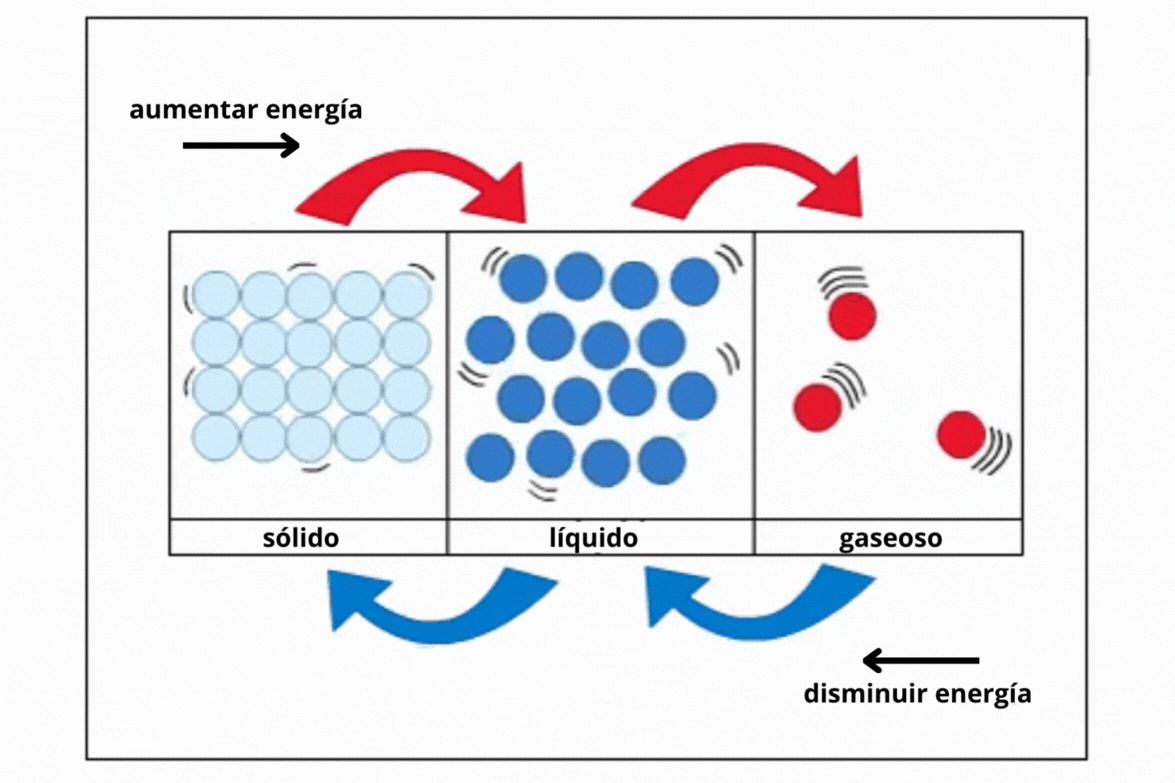
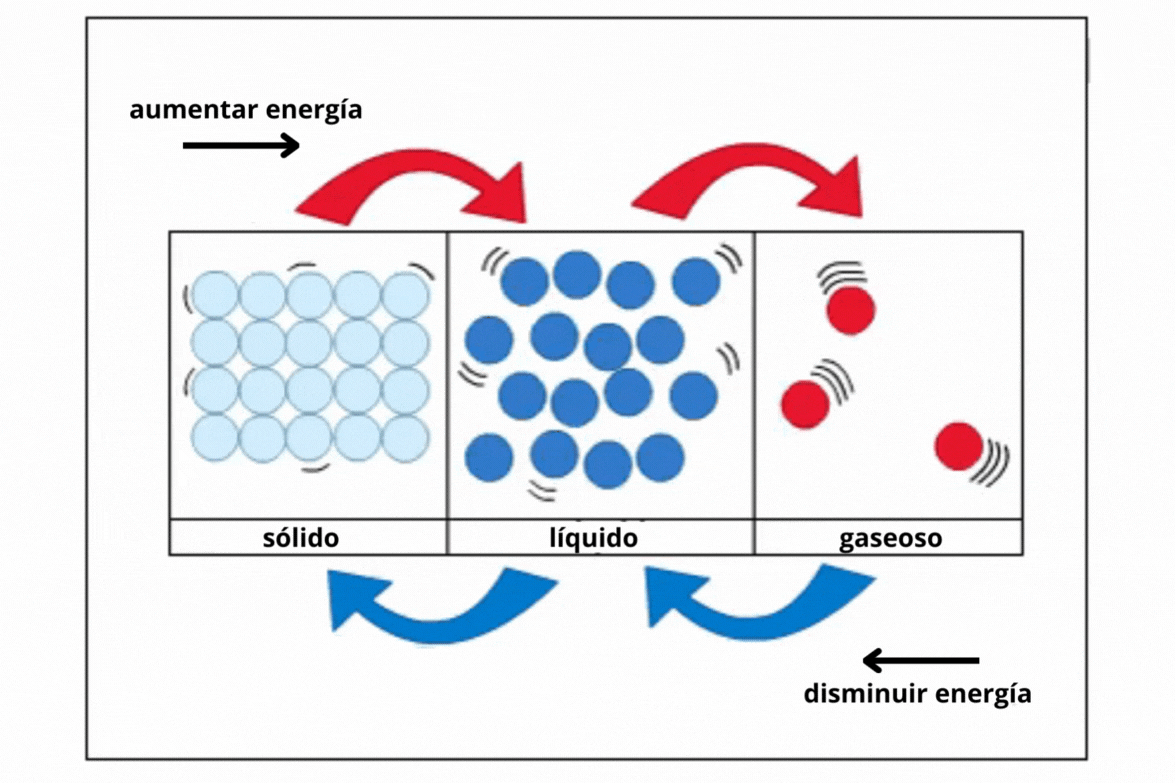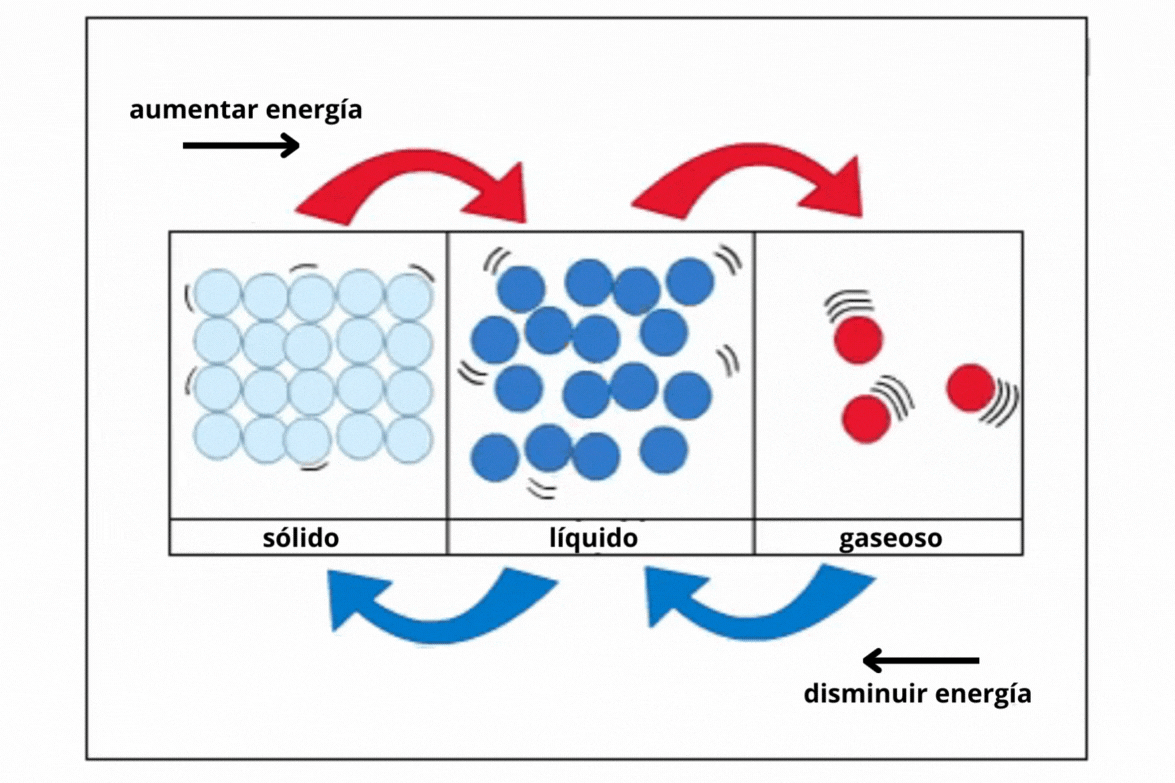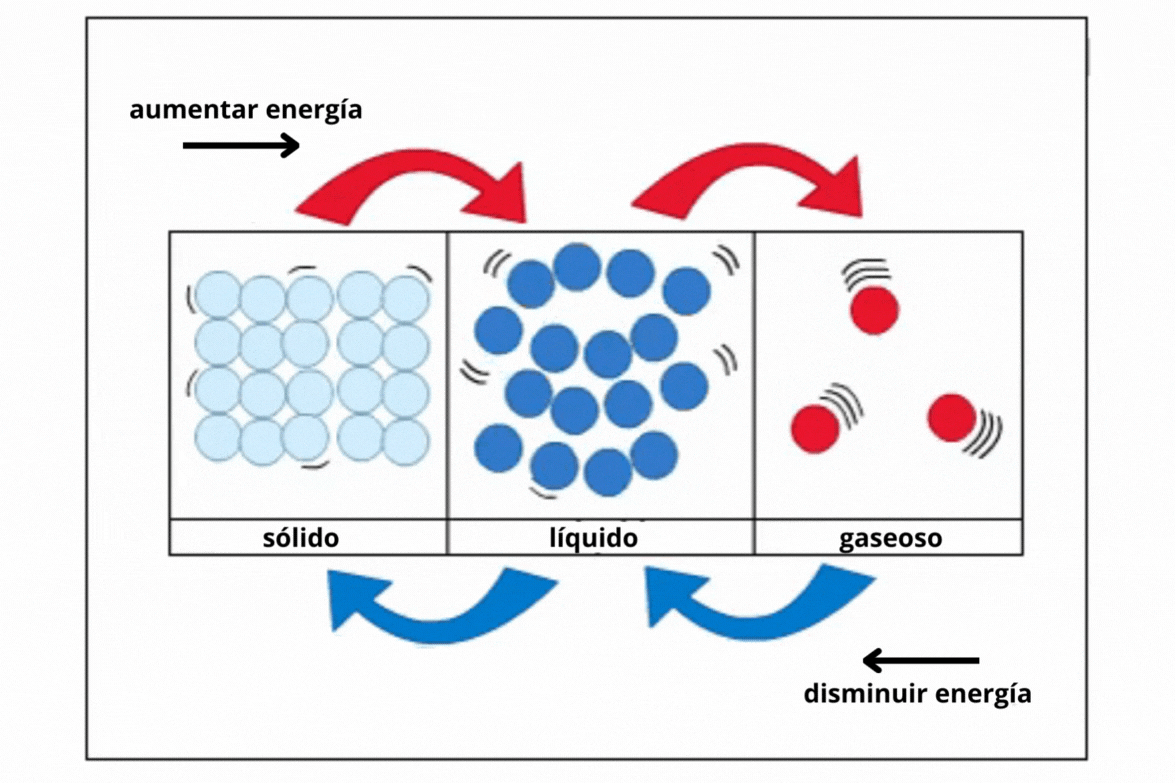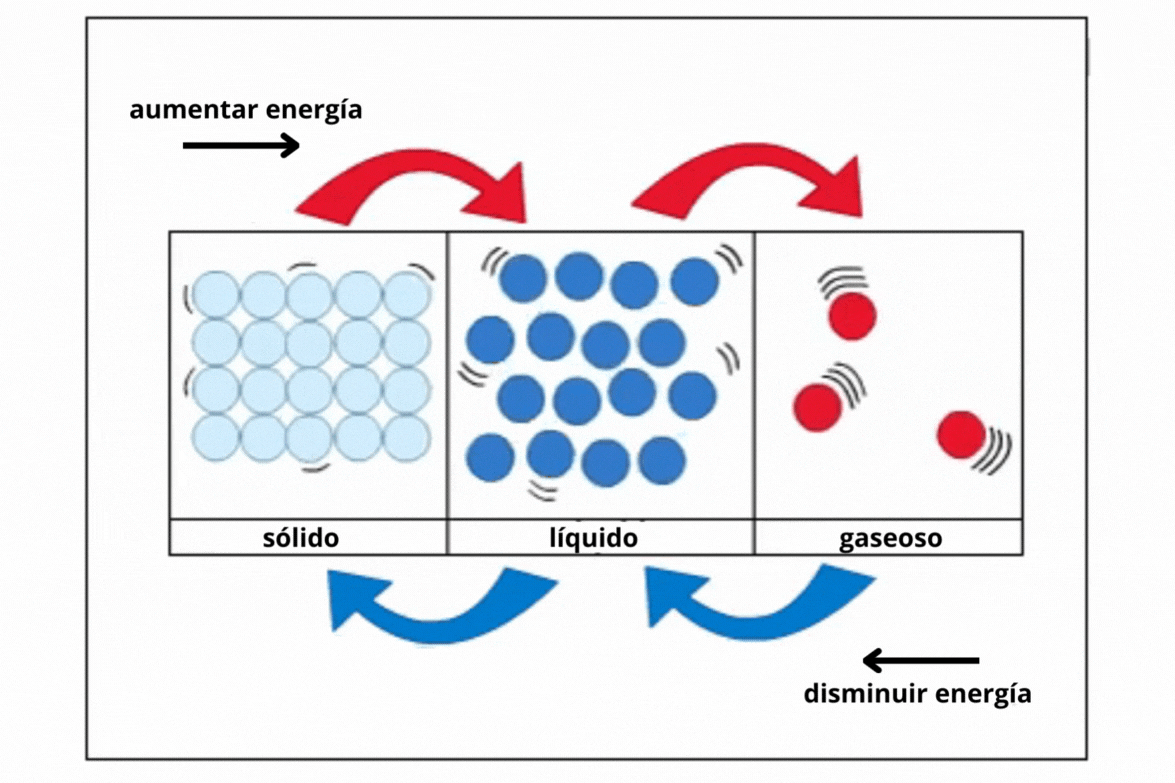
Estado de agregación |
F |
|---|
Fase |
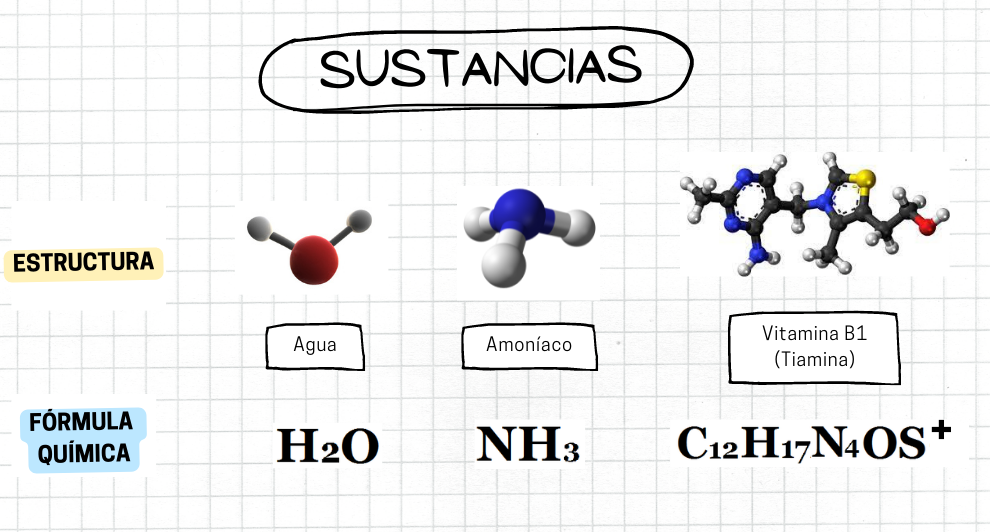
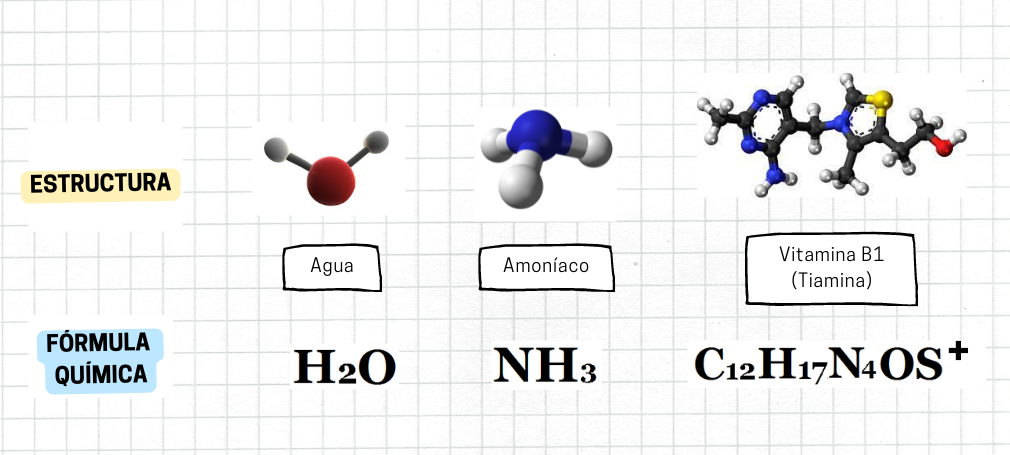
Fórmula QuímicaLa
fórmula química es una forma de representar a una sustancia. La
fórmula química muestra la composición
química
de
la sustancia. La fórmula química utiliza símbolos químicos y subíndices numéricos. Los subíndices numéricos representan las cantidades relativas (proporciones) de los átomos de los diferentes elementos que forman la sustancia Por ejemplo, la fórmula química del agua es H₂O, y muestra que el agua está compuesta por los elementos hidrógeno y oxígeno, en proporción relativa 2 a 1.
 |
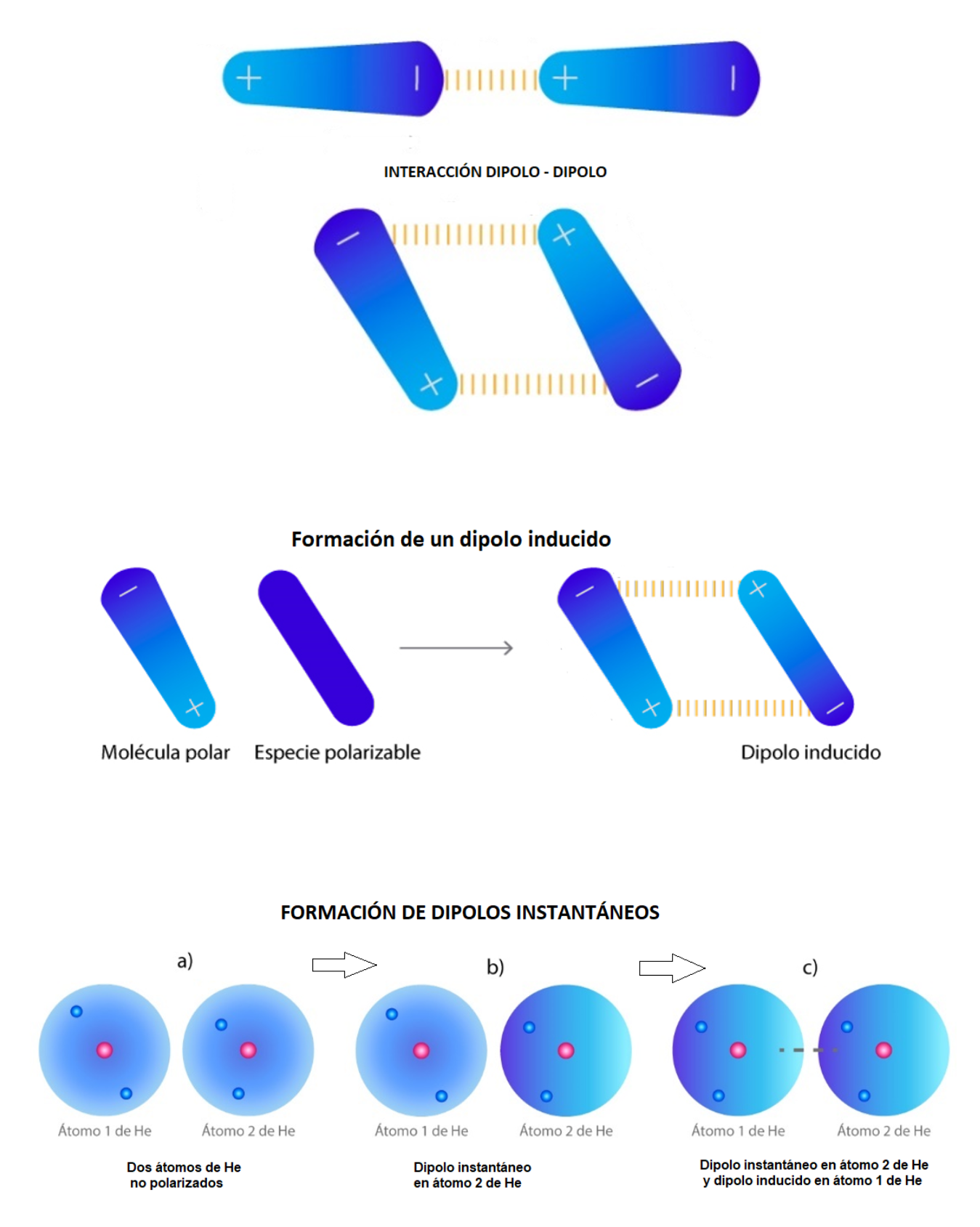
Fuerzas De Van der WaalsLas
fuerzas de Van der Waals son un tipo de enlace de baja energía que
se establece entre las moléculas. Las fuerzas de Van der Waals son las fuerzas de atracción o fuerzas de repulsión entre las moléculas. Existen tres tipos de fuerzas de Van der Waals:
 |
G |
|---|
Gas |
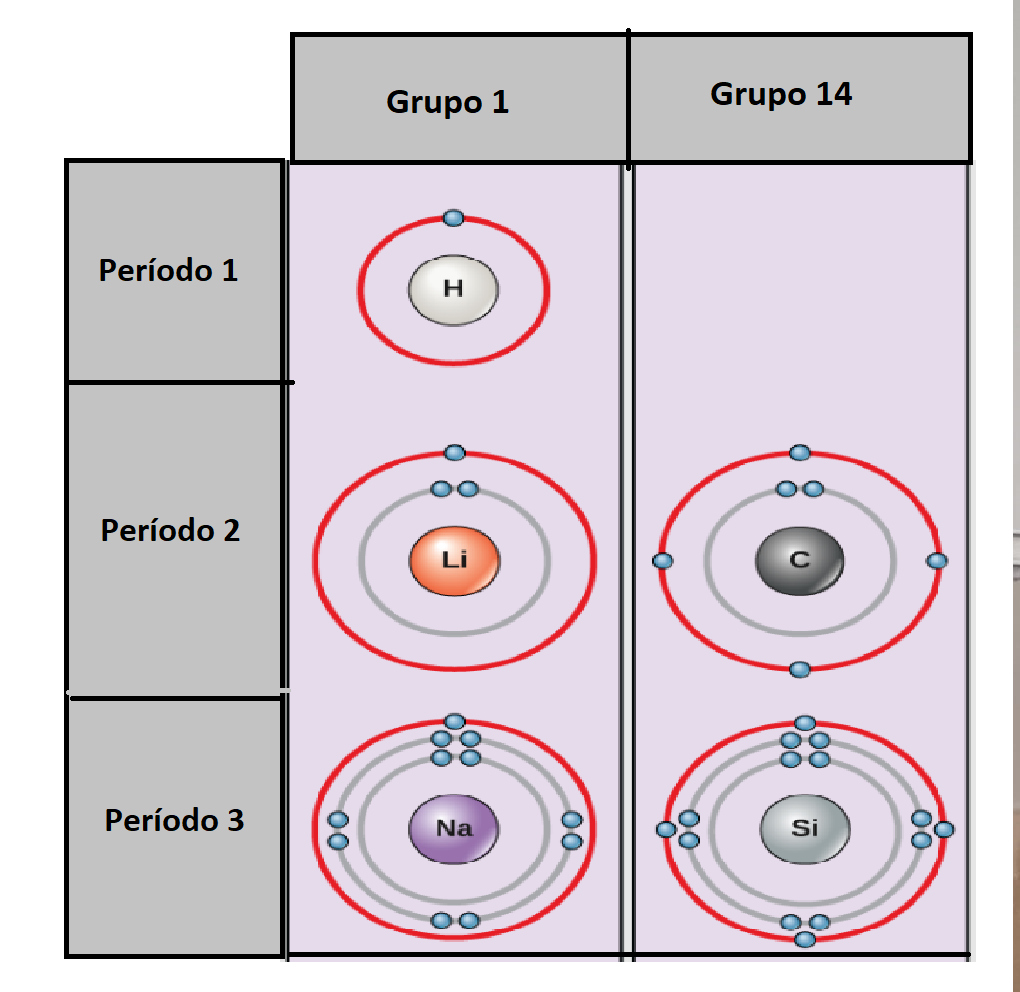
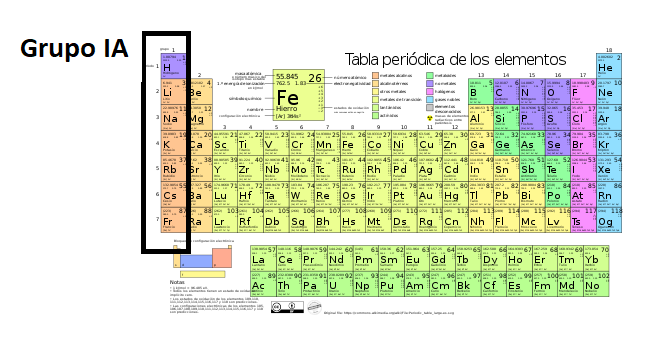
Grupo en la Tabla PeriódicaLos
grupos son las columnas de la tabla
periódica.
La tabla periódica tiene 18 grupos. Los elementos en cada grupo tienen propiedades químicas similares.
 |
I |
|---|
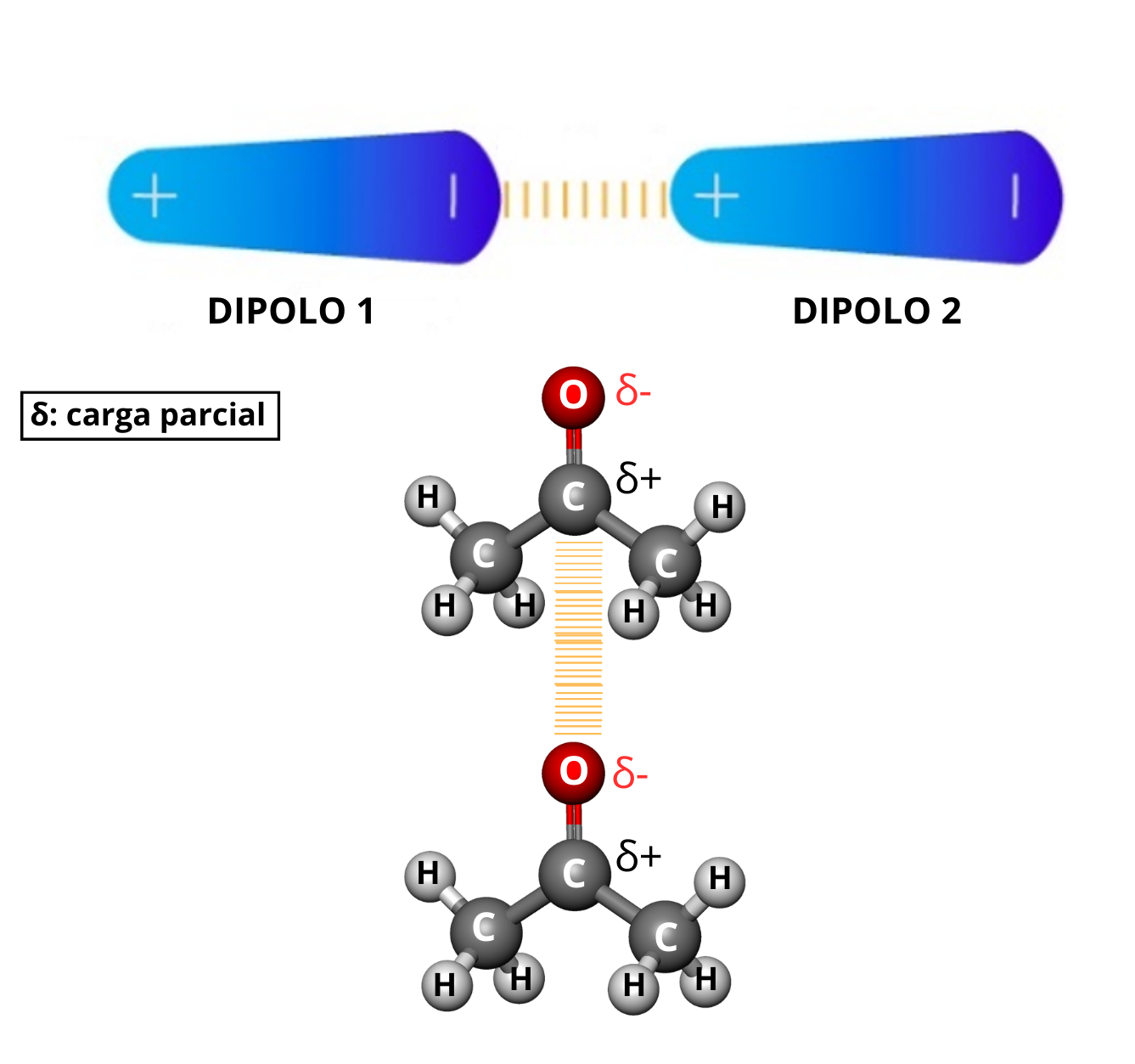
Interacción Dipolo - Dipolo (Fuerzas de Keesom)La interacción dipolo - dipolo se establece cuando una molécula polar (dipolo 1) se aproxima a otra molécula polar (dipolo 2). Esta interacción dipolo-dipolo mantiene unidas a las dos moléculas. La fuerza de la interacción dipolo - . dipolo depende:
|
INTERACCIÓN DIPOLO-DIPOLO (FUERZAD DE DEBYE)
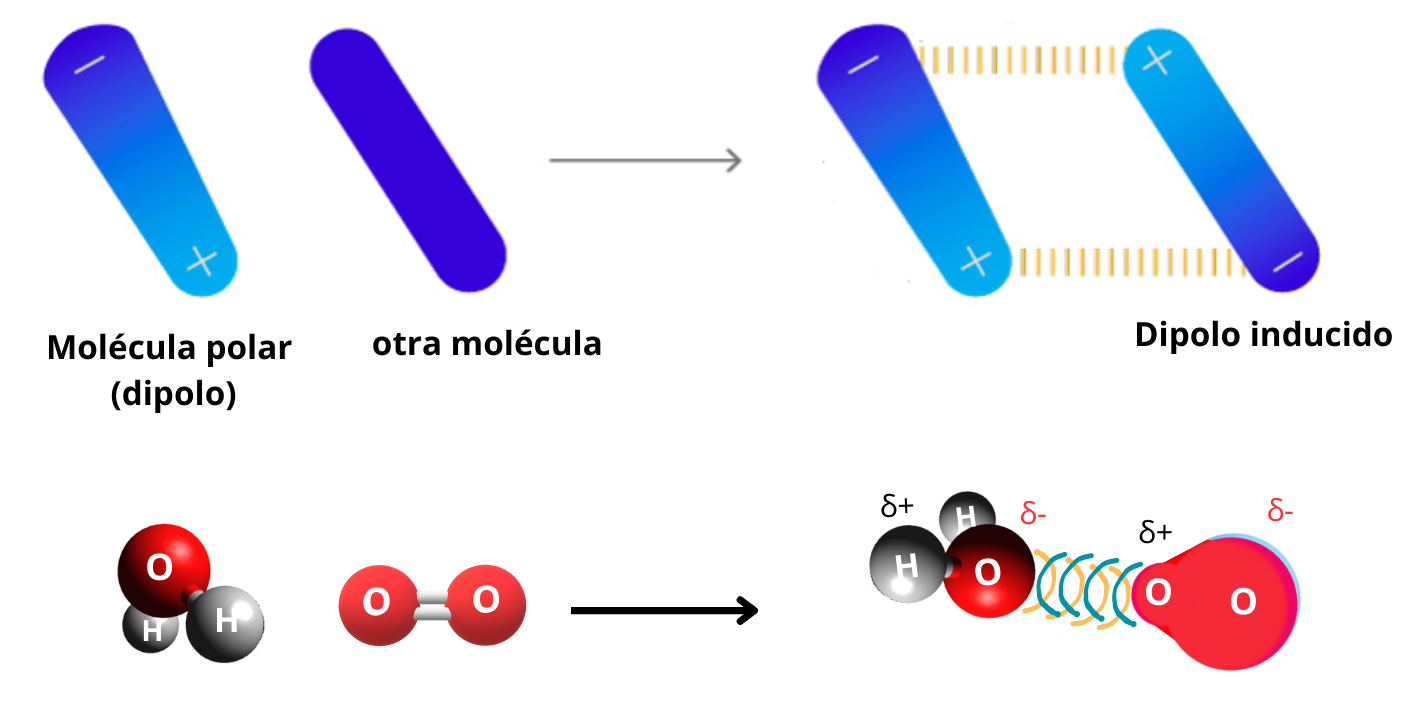
Interacción Dipolo - Dipolo Inducido (Fuerzas de Debye). La interacción dipolo - dipolo inducido se establece cuando una molécula polar (dipolo) se aproxima a otra molécula generando un dipolo en esta otra molécula (dipolo inducido). Esta interacción dipolo-dipolo inducido, mantiene unidas a las dos moléculas. La fuerza de la interacción dipolo - . dipolo inducido depende de:
 |
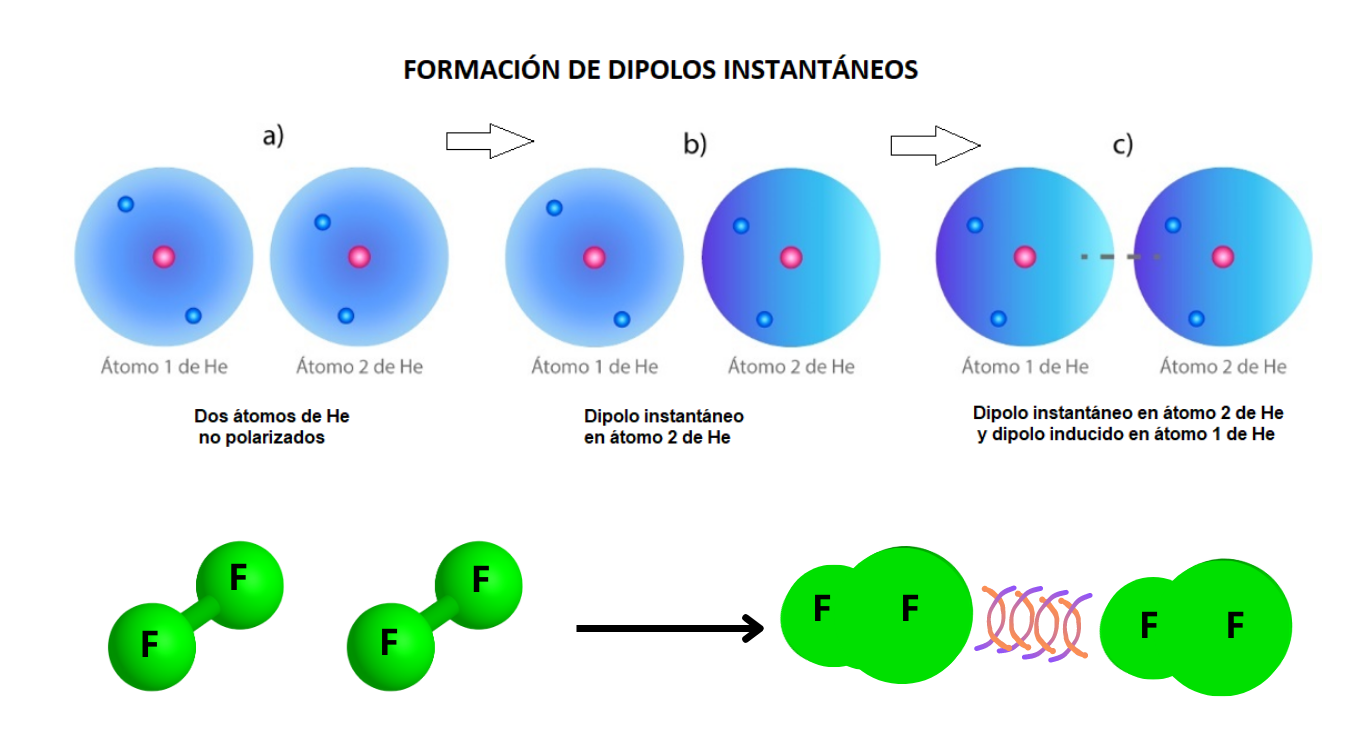
INTERACCIÓNDIPOLO INSTANTÁNEO-DIPOLO INDUCIDO (FUERZAS DE LONDON)zas de London)Interacción Dipolo Instantáneo - Dipolo Inducido (Fuerzas de London). La interacción dipolo instantáneo- dipolo inducido se establece cuando una molécula con un dipolo instantáneo genera un dipolo en otra molécula que está cerca (dipolo inducido). Un dipolo instantáneo se genera por cambios rápidos en la distribución de los electrones en la molécula. Los dipolos instantáneos generan atracciones entre las moléculas incluso cuando las moléculas no son polares.
|
Ion |
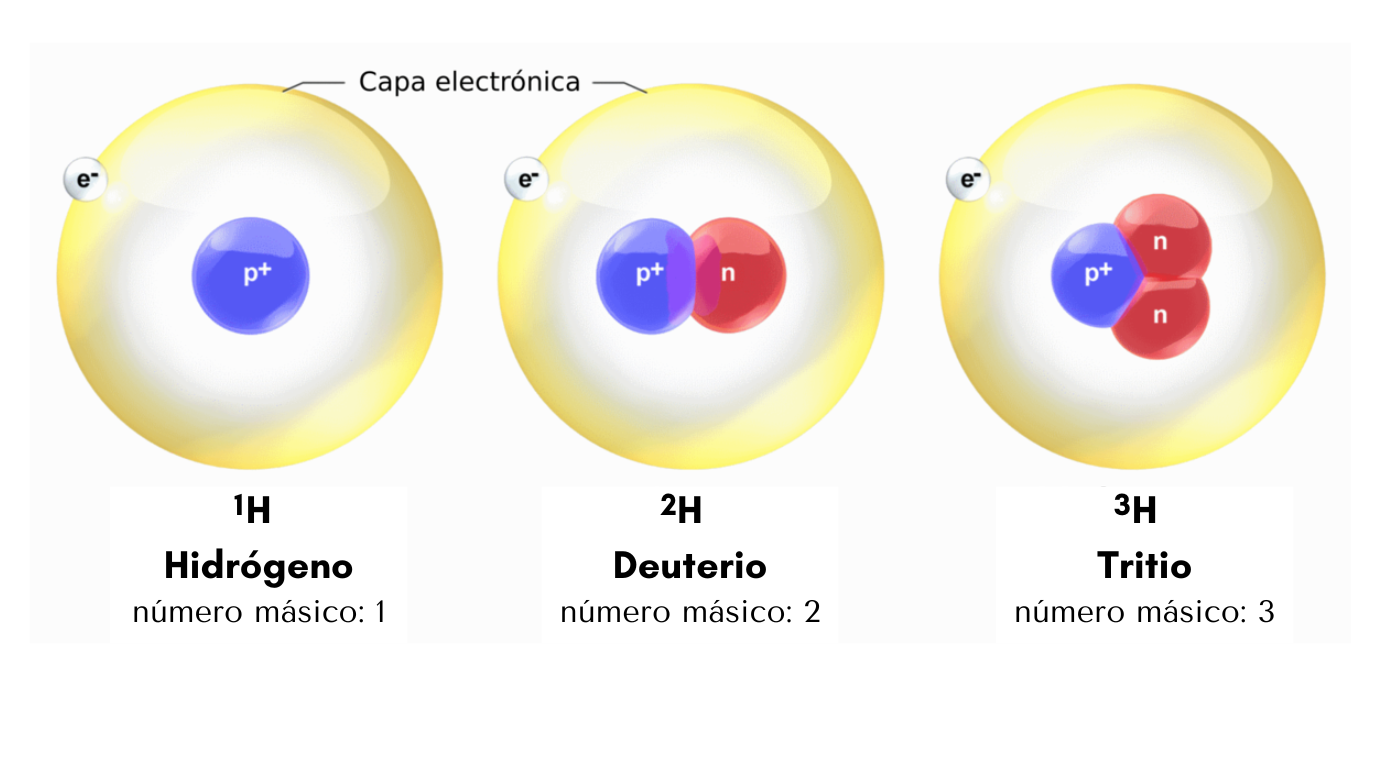
IsótoposLos
isótopos son átomos
de
un mismo elemento con diferente número
másico. Los isótopos tienen igual número de protones pero diferente número de neutrones. Por ejemplo, el elemento hidrógeno posee tres isótopos. El isótopo más abundante es el 1H que tiene un protón. Otro isótopo, el 2H, tiene 1 protón y 1 neutrón. El otro isótopo, el 3H, tiene 1 protón y 2 neutrones.
 |
L |
|---|
Líquido |
M |
|---|
Magnitud |
Masa |
MateriaLa materia es el material físico del universo. La materia es lo que compone todo lo que está a nuestro alrededor. La materia tiene masa y volumen. Hay diferentes tipos de materia. Por ejemplo, algunos tipos de materia son las sustancias, como los elementos y los compuestos. Otro tipo de materia son las mezclas. 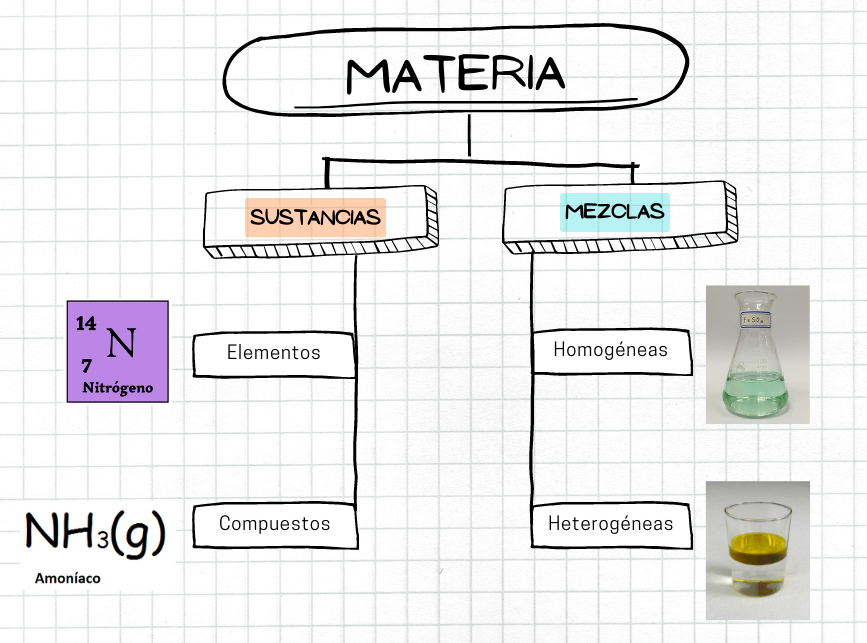 |
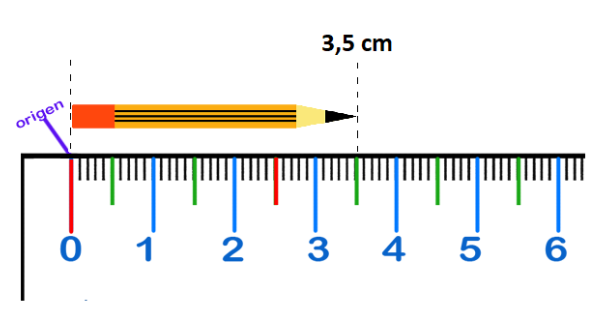
MediciónLa
medición es el proceso de comparar una cantidad desconocida que
queremos determinar con una cantidad conocida de la misma magnitud,
que se usa como referencia o unidad. Al resultado del proceso de medición se le llama medida. |
Medida |
MezclaUna mezcla es un tipo de materia que está formada por dos o más sustancias. En una mezcla, cada sustancia conserva su composición química. Las sustancias tienen composición química fija. En cambio, la composición de una mezcla puede variar. Existen dos tipos de mezclas: las mezclas homogéneas y las mezclas heterogéneas.
|
Mezcla Heterogénea |
Mezcla Homogénea |
MoléculaLa
molécula es la unión de dos o más átomos. La unión de los átomos
en
las moléculas se da por enlaces
químicos. Los átomos que forman la molécula pueden ser del mismo elemento químico o de distintos elementos químicos. Las moléculas tienen propiedades físicas y químicas que las caracterizan. Un ejemplo de molécula es la molécula de agua. Su fórmula química es H2O. Está compuesta por un átomo de oxígeno y dos átomos de hidrógeno unidos por enlaces covalentes.
 |
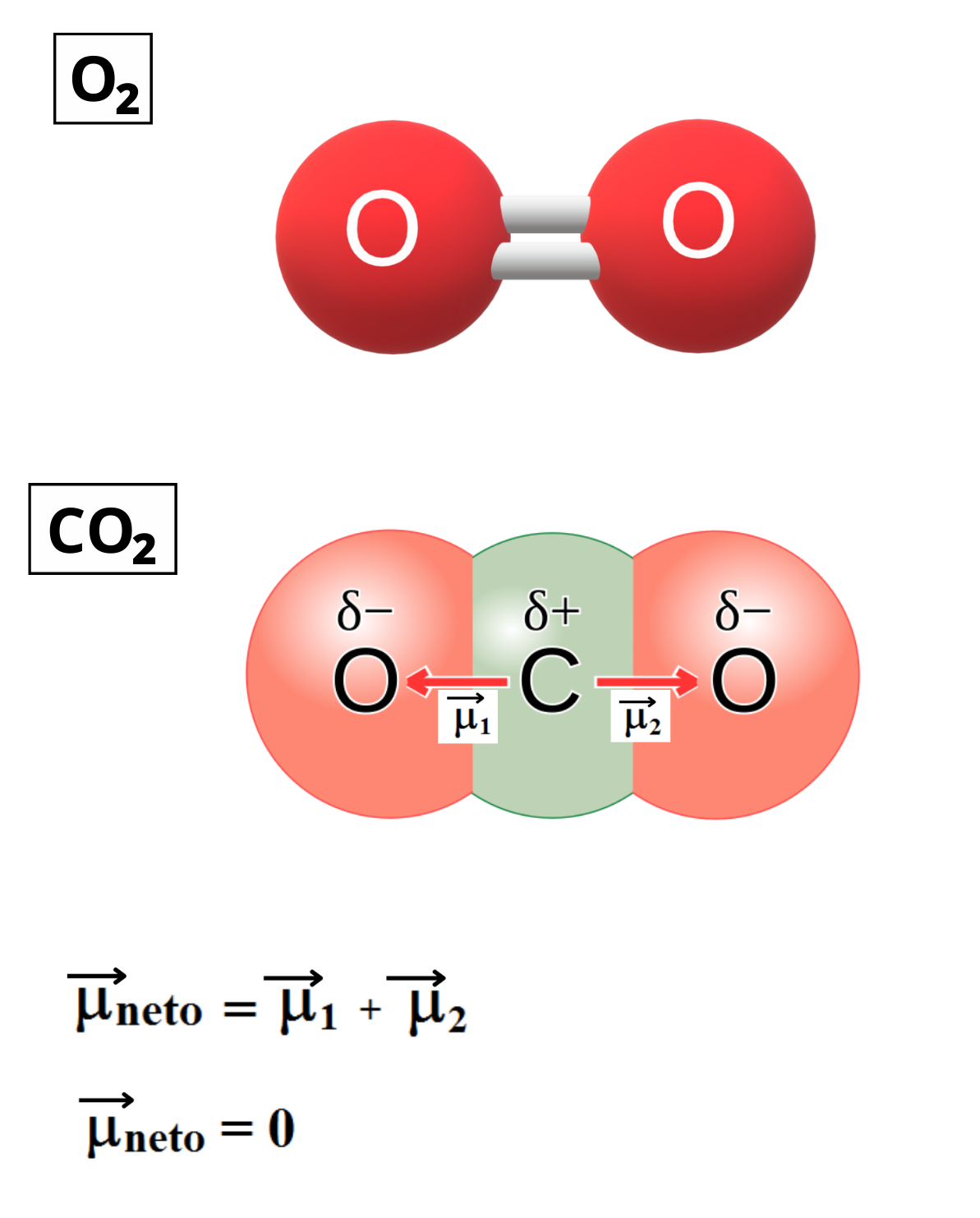
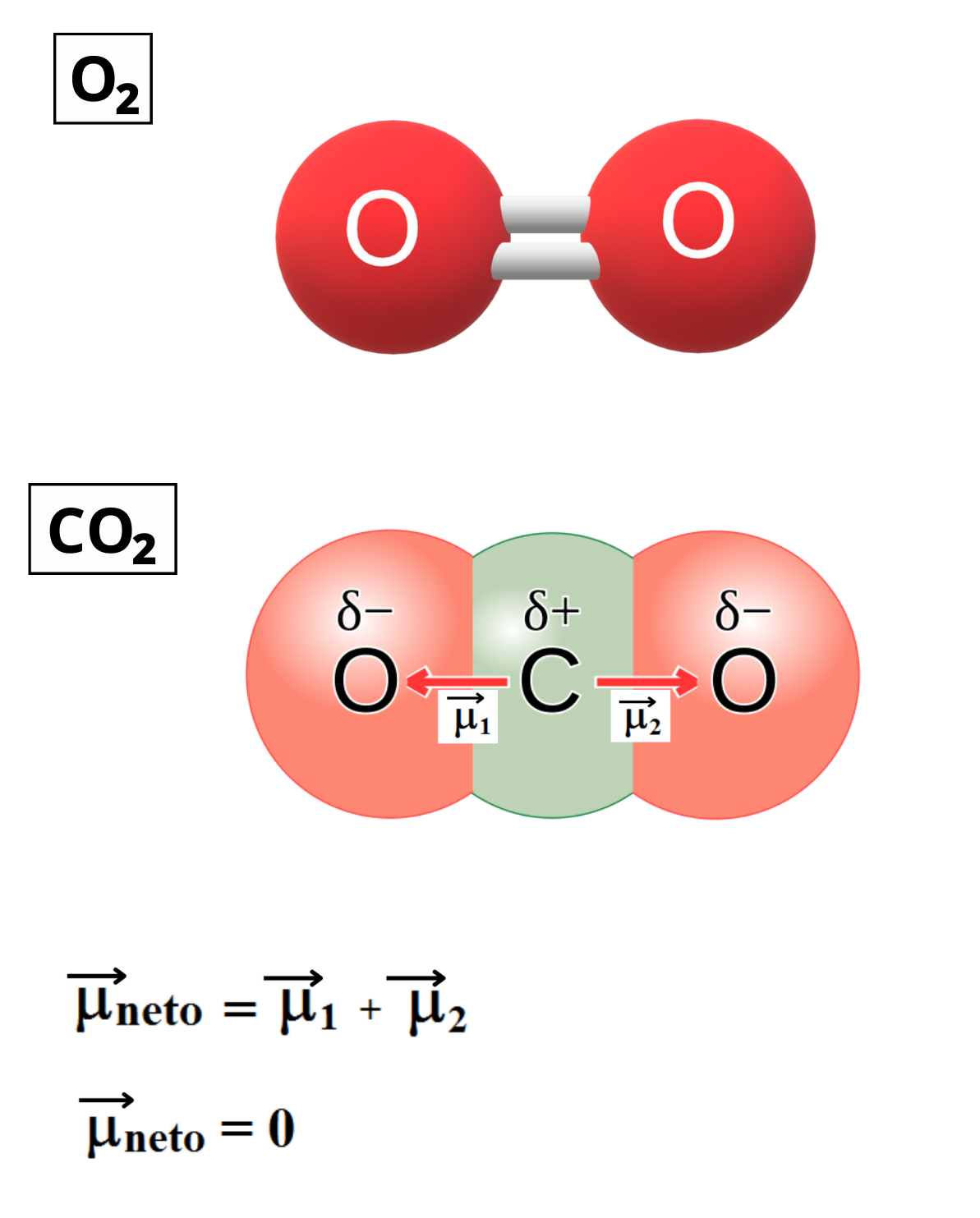
MOLÉCULA APOLAR
Molécula Apolar. Una molécula es apolar si su momento dipolar neto es igual a cero. Las moléculas que no presentan regiones con cargas parciales son apolares (Ejemplo: molécula de oxígeno). Las moléculas que tienen enlaces polares son apolares cuando el momento dipolar neto es cero (Ejemplo: molécula de dióxido de carbono).
|
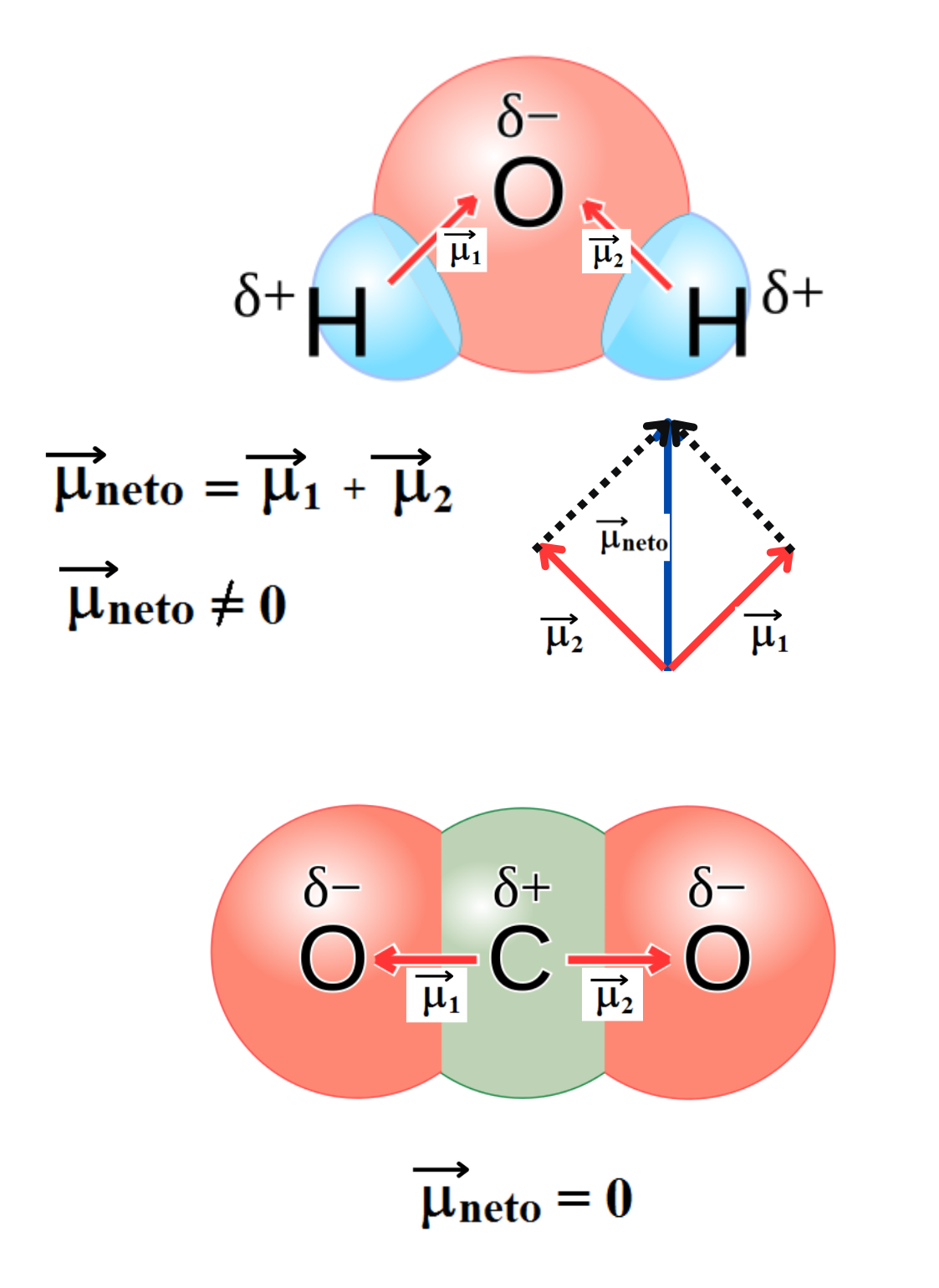
MOLÉCULA POLAR |
MOMENTO DIPOLAR
Momento Dipolar. El momento dipolar se define como el producto entre las cargas y la distancia entre dichas cargas. El momento dipolar es una magnitud vectorial. NOTA: En química es común representar el momento dipolar con un vector (flecha) que apunta desde la carga parcial positiva hacia la carga parcial negativa. En la convención moderna y en física, el vector apunta hacia la carga parcial positiva.
|
N |
|---|
NeutrónUn
neutrón es una partícula sin carga. El neutrón se encuentra en el
núcleo
del
átomo. La cantidad de neutrones en el núcleo define el isótopo del elemento. Por ejemplo, el elemento nitrógeno posee dos isótopos. Un isótopo,
14N, tiene átomos
con
7 protones
y
7 neutrones. El otro isótopo,
15N, tiene átomos
con
7 protones
y
8 neutrones.
|
Núcleo del Átomo |
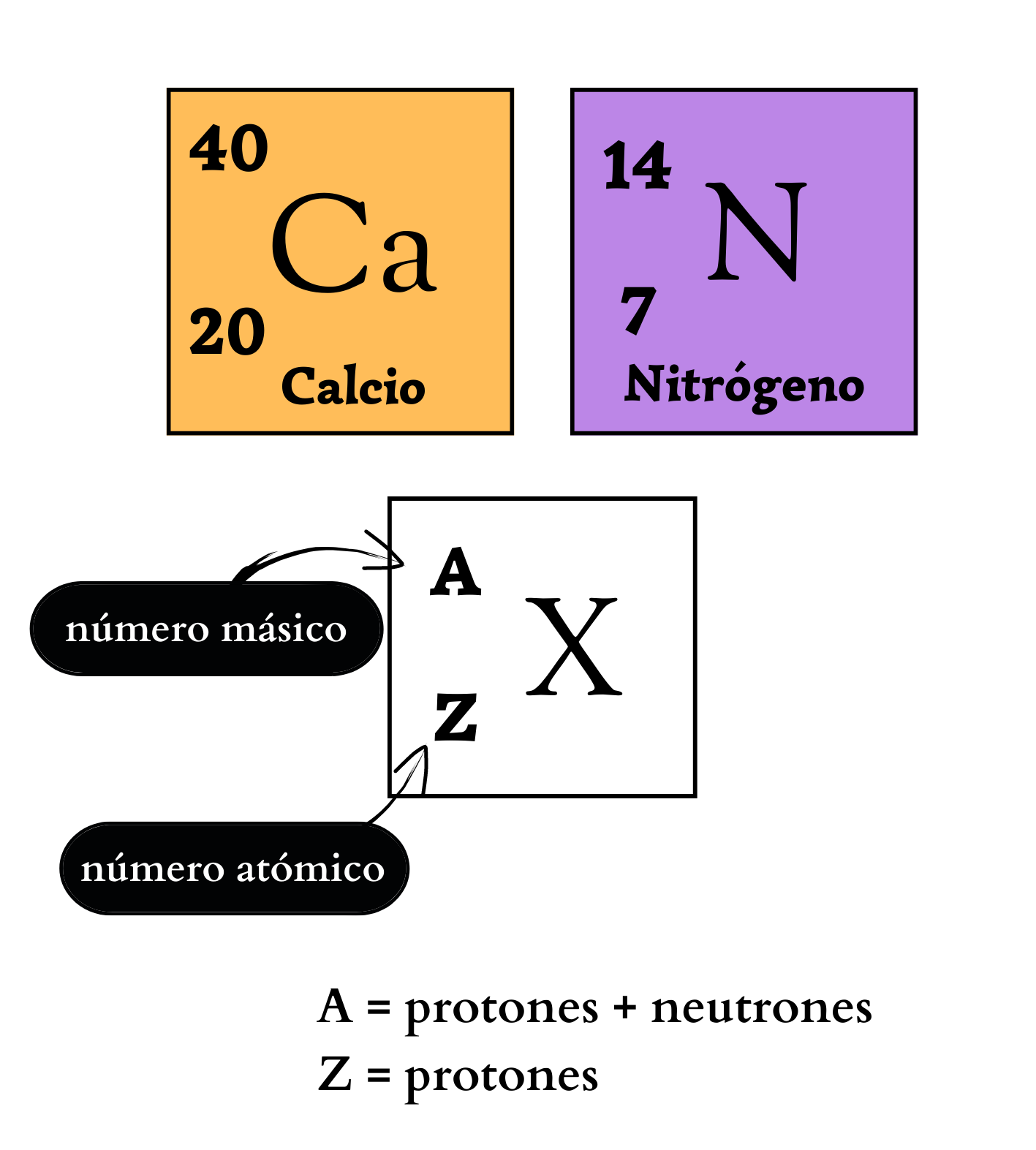
Número AtómicoEl
número atómico indica la cantidad de protones
que
tiene un átomo
de
un elemento
en
el núcleo. El número atómico define al elemento. Por ejemplo, todos los átomos del elemento nitrógeno tienen número atómico igual a 7, por lo que poseen 7 protones en su núcleo. En cambio, todos los átomos del elemento calcio tienen número atómico igual a 20, por lo que poseen 20 protones en su núcleo.
 |
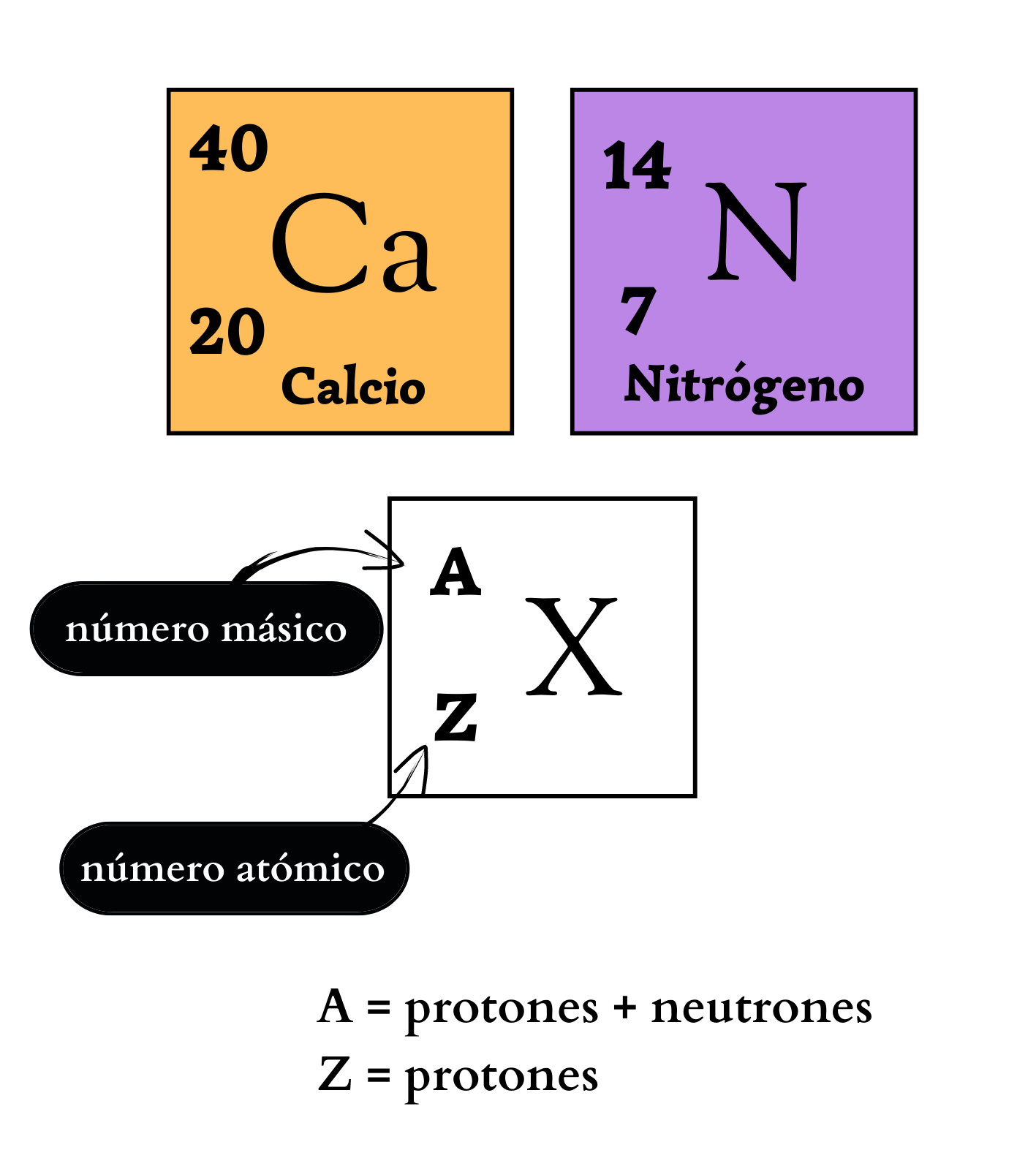
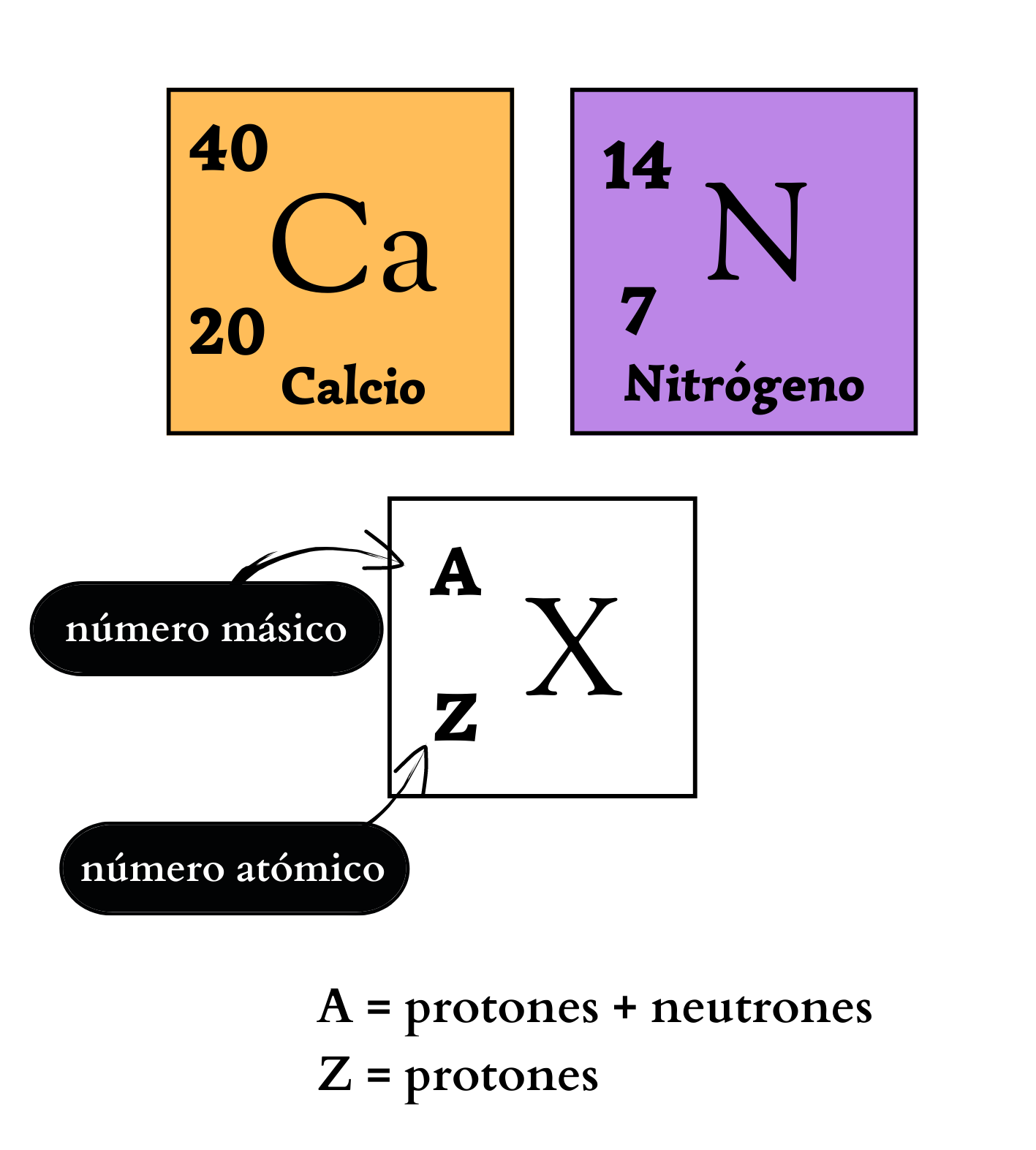
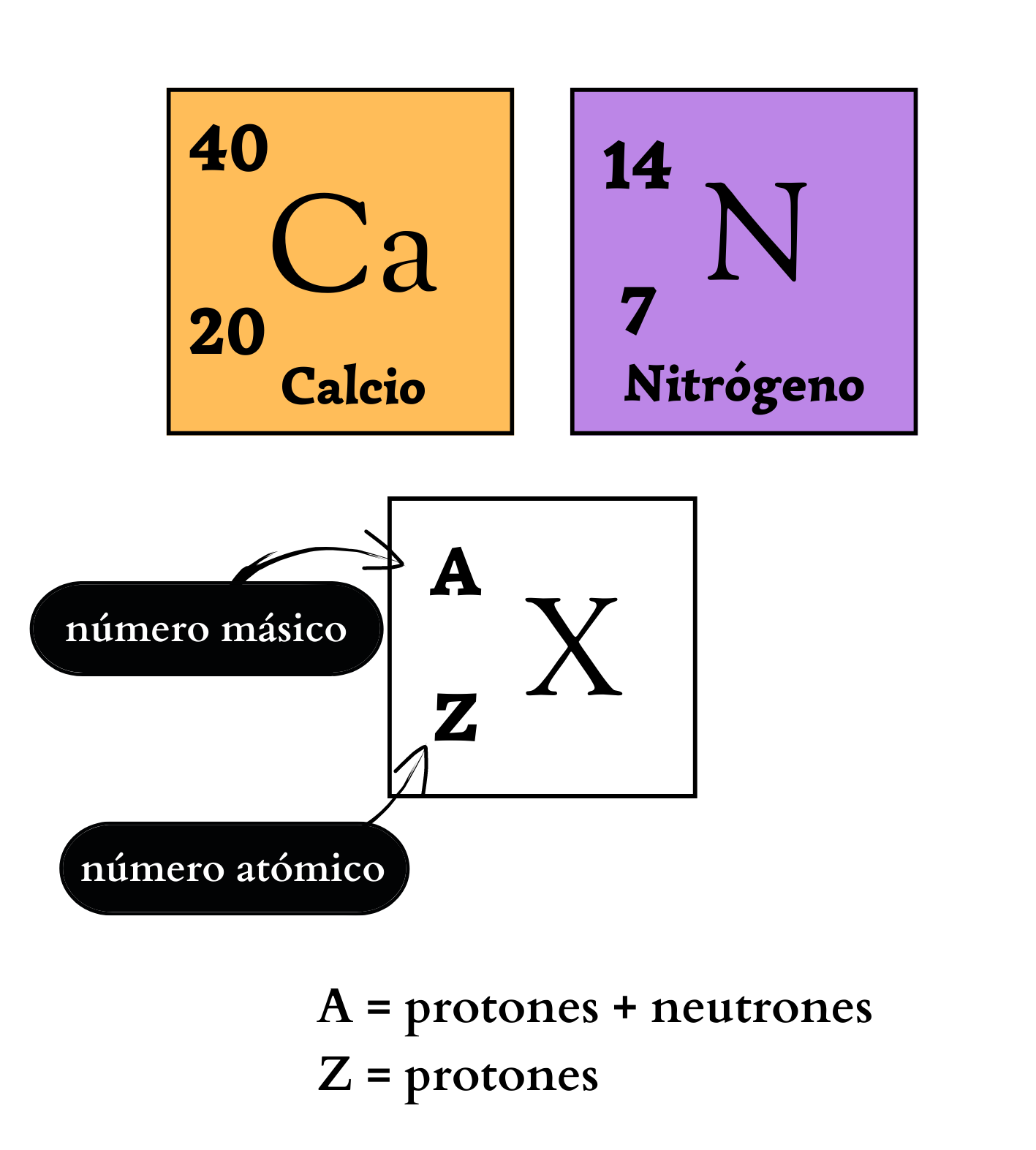
Número MásicoEl
número másico de un átomo
indica
la cantidad de protones
y
neutrones
que
tiene el núcleo
atómico. El número másico se simboliza con la letra A y se coloca a la izquierda y arriba del símbolo químico del elemento. Por ejemplo, los átomos más abundantes del elemento nitrógeno se simbolizan como 14N, poseen 7 protones y 7 neutrones. Los átomos de un mismo elemento con diferente número másico se llaman isótopos. Los isótopos tienen igual número de protones pero diferente número de neutrones. Por ejemplo, el elemento nitrógeno posee dos isótopos. Un isótopo, 14N, tiene átomos con 7 protones y 7 neutrones. El otro isótopo, 15N tiene átomos con 7 protones y 8 neutrones.
 |
O |
|---|
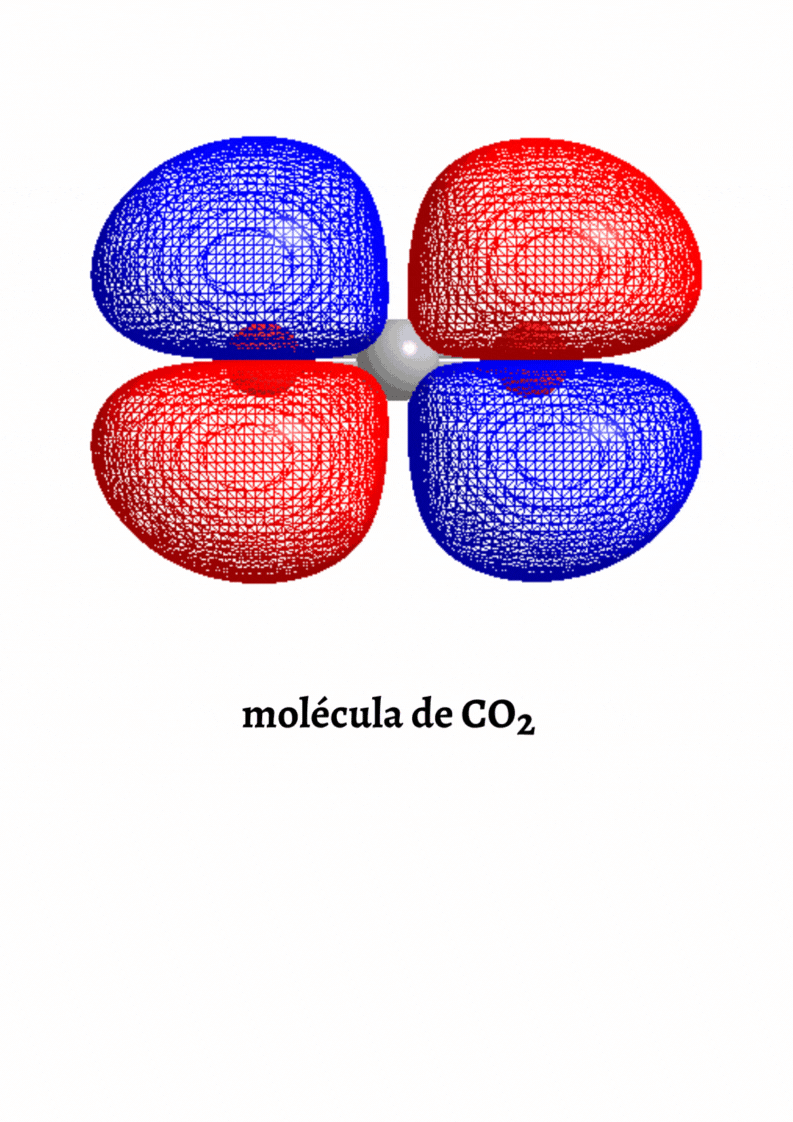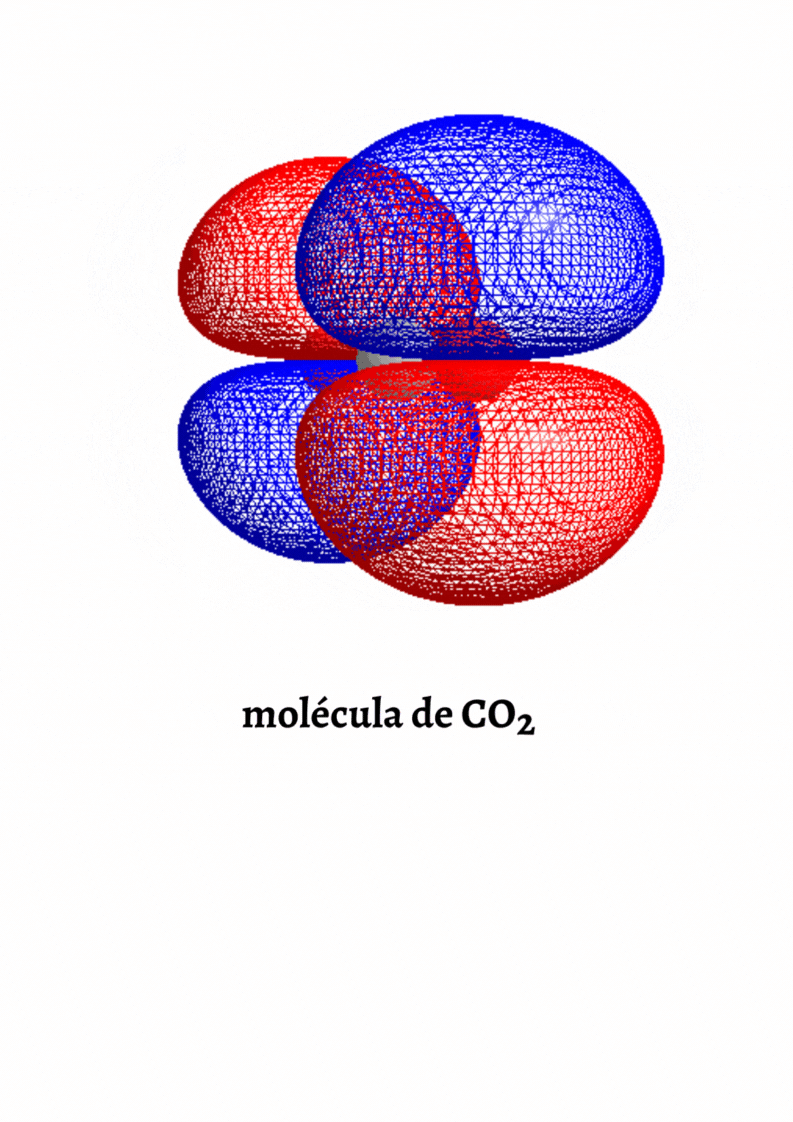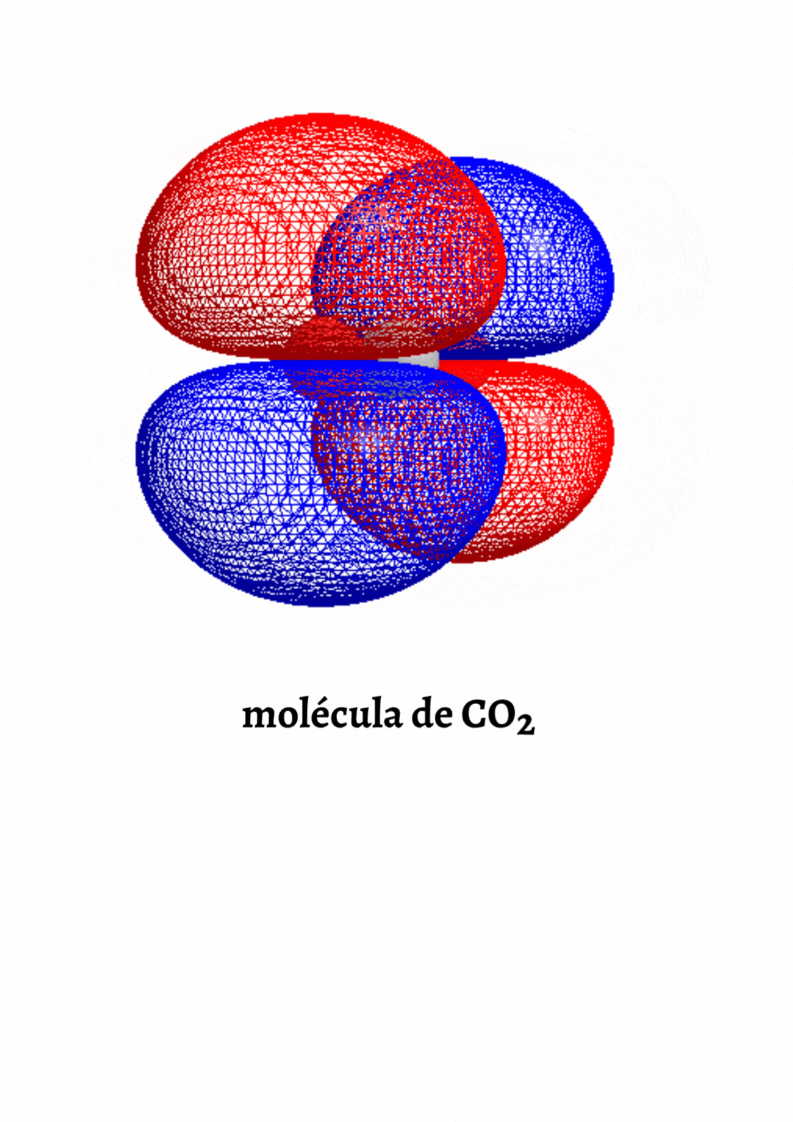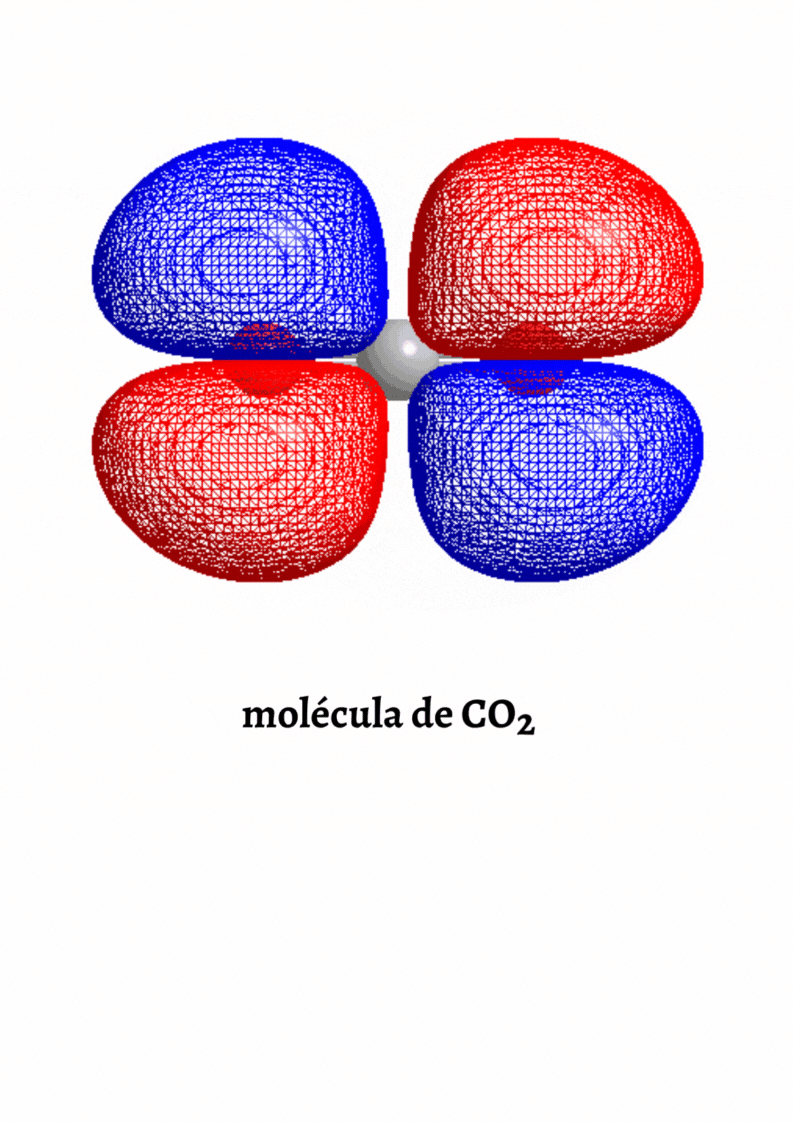
Orbital atómico
Orbital atómico Un orbital atómico es un orbital asociado a un átomo. Algunos tipos de orbitales atómicos son los orbitales s y los orbitales p. 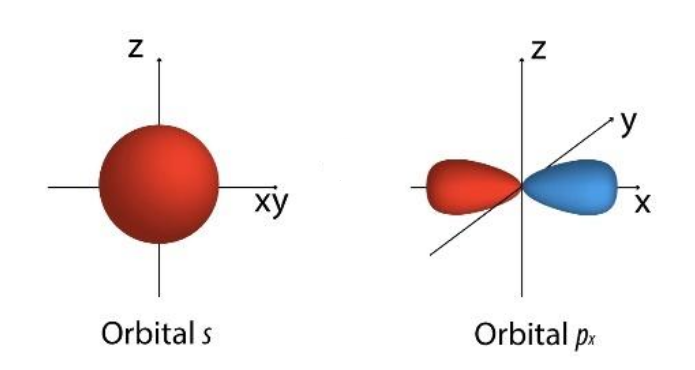 |
Orbital Molecular |
P |
|---|
PartículaLa partícula es un fragmento pequeño de materia. Algunas partículas, son tan pequeñas que no podemos verlas a simple vista. Ejemplos: átomos y moléculas.
|
Periferia AtómicaLa periferia atómica es la zona del átomo que rodea al núcleo atómico. En la periferia atómica se encuentran los electrones. La periferia atómica tiene una región interna, más cercana al núcleo. La periferia atómica tiene una región externa más alejada del núcleo. En la región interna están los electrones internos del átomo. En la región externa de la periferia están los electrones de valencia del átomo. Los electrones de valencia son los electrones que participan en el enlace químico.
|
Período en la Tabla PeriódicaLos
períodos son las filas de la tabla periódica. La tabla
periódica
tiene
7 períodos.
|
ProductosLos
productos son las sustancias
que
se obtienen en una
reacción
química. Los productos aparecen a la derecha de la flecha en una ecuación química.  |
Propiedades QuímicasLas
propiedades químicas describen la forma en que una sustancia
puede
cambiar o reaccionar para formar otras sustancias. Ejemplos:
|
ProtónUn protón es una partícula de carga positiva. El protón se encuentra
en el núcleo
del
átomo. La cantidad de protones en el núcleo define al elemento. Por ejemplo, todos los átomos del elemento nitrógeno poseen 7 protones en su núcleo. En cambio, todos los átomos del elemento calcio poseen 20 protones en su núcleo.
 |
Puente de HidrógenoEl
puente de Hidrógeno es la denominación antigua del enlace
de Hidrógeno.
|
R |
|---|
Reacción química |
ReactivosLos
reactivos son las sustancias
de
partida en una reacción
química. Los reactivos aparecen a la izquierda de la flecha en una ecuación química.  |
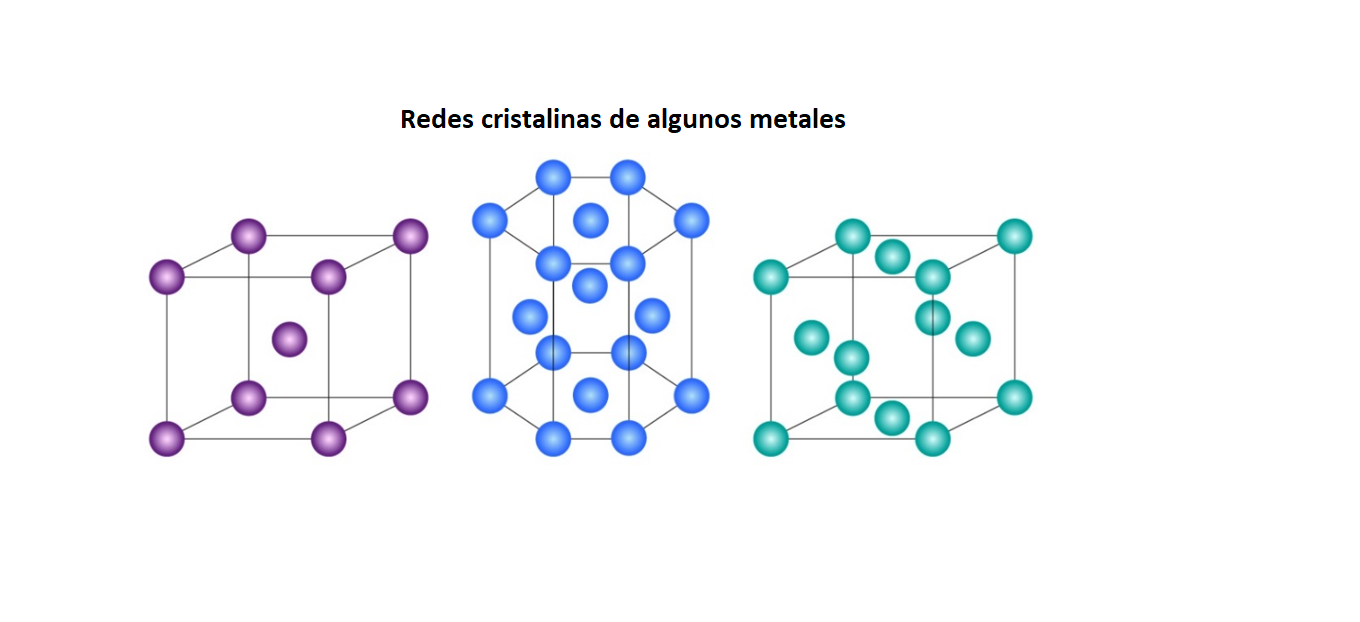
Red CristalinaUna
red cristalina es un sólido
formado
por átomos,
iones
o
moléculas. Los átomos, iones o moléculas de la red cristalina están ordenados en el espacio de forma repetida. Un ejemplo de red cristalina son los metales.
|
S |
|---|
Símbolo QuímicoEl
símbolo químico es una forma de representar a un elemento
químico
con
letras. Cada elemento químico se representa con un símbolo químico formado por una letra mayúscula o por dos letras, una mayúscula y una minúscula. Por ejemplo, el elemento nitrógeno se representa como N, y el elemento calcio como Ca. El símbolo químico, además de las letras, puede incluir el número másico y el número atómico. Cada elemento químico se compone de un solo tipo de átomo.
|
SistemaUn
sistema es la porción del Universo que nos interesa estudiar Algunos ejemplos de sistemas son:
|
Sistema Heterogéneo |
Sistema Homogéneo |
Sólido |
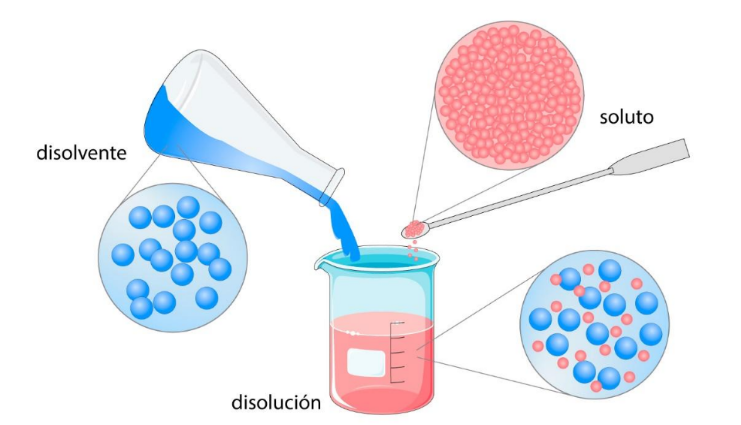
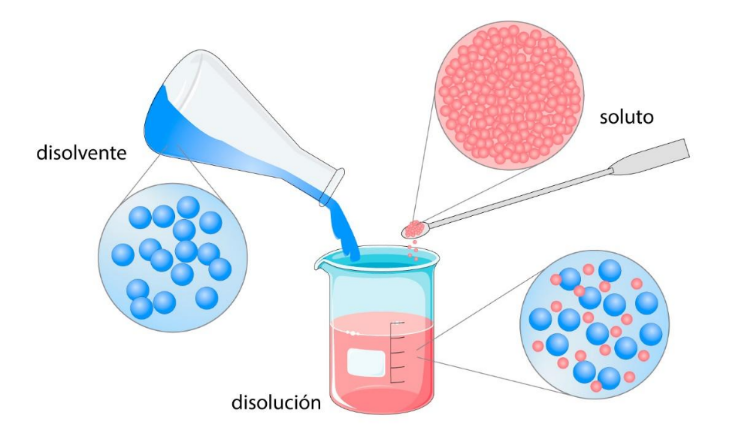
SolutoEs
una sustancia disuelta en un disolvente
para
formar una disolución. En general el soluto está en menor proporción que el disolvente. 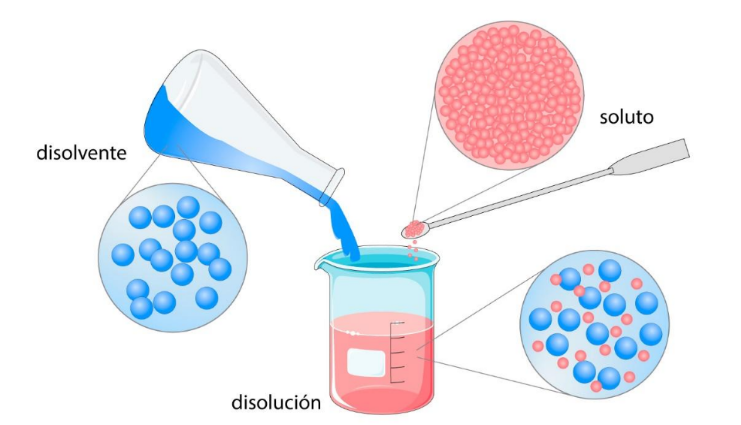 |
SustanciaLa sustancia es un tipo de materia que tiene composición fija y propiedades definidas. Si se modifica la composición química de una sustancia se transforma en una nueva sustancia. Un sistema que contiene dos o más sustancias es una mezcla
|
SUSTANCIA IÓNICA |
T |
|---|
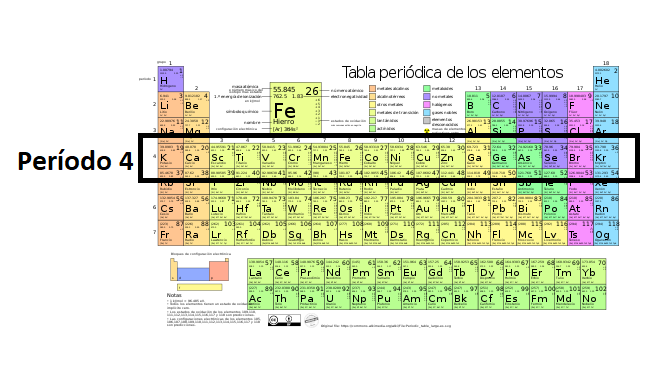
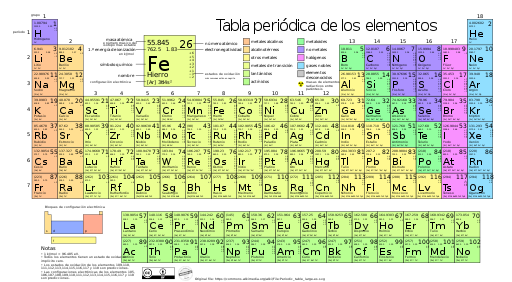
Tabla Periódica de los Elementos QuímicosLa
tabla periódica es una forma de organizar los elementos
químicos. En la tabla periódica los elementos químicos se encuentran ordenados por su número atómico y por sus propiedades químicas. La tabla periódica está compuesta por casillas ordenadas en filas y columnas. Las filas son llamadas períodos y las columnas son llamadas grupos. En cada casilla se representa un elemento químico con su símbolo químico e información del elemento químico.
 |
V |
|---|
VolumenEl volumen es la medida del espacio que ocupa un objeto. En el Sistema Internacional, la unidad de medida del volumen es el metro cúbico (m3) y 1 m3 = 1000 L
|