GLOSARIO DE QUÍMICA
GLOSARIO DE QUÍMICA
Especial | A | B | C | D | E | F | G | H | I | J | K | L | M | N | Ñ | O | P | Q | R | S | T | U | V | W | X | Y | Z | TODAS
I |
|---|
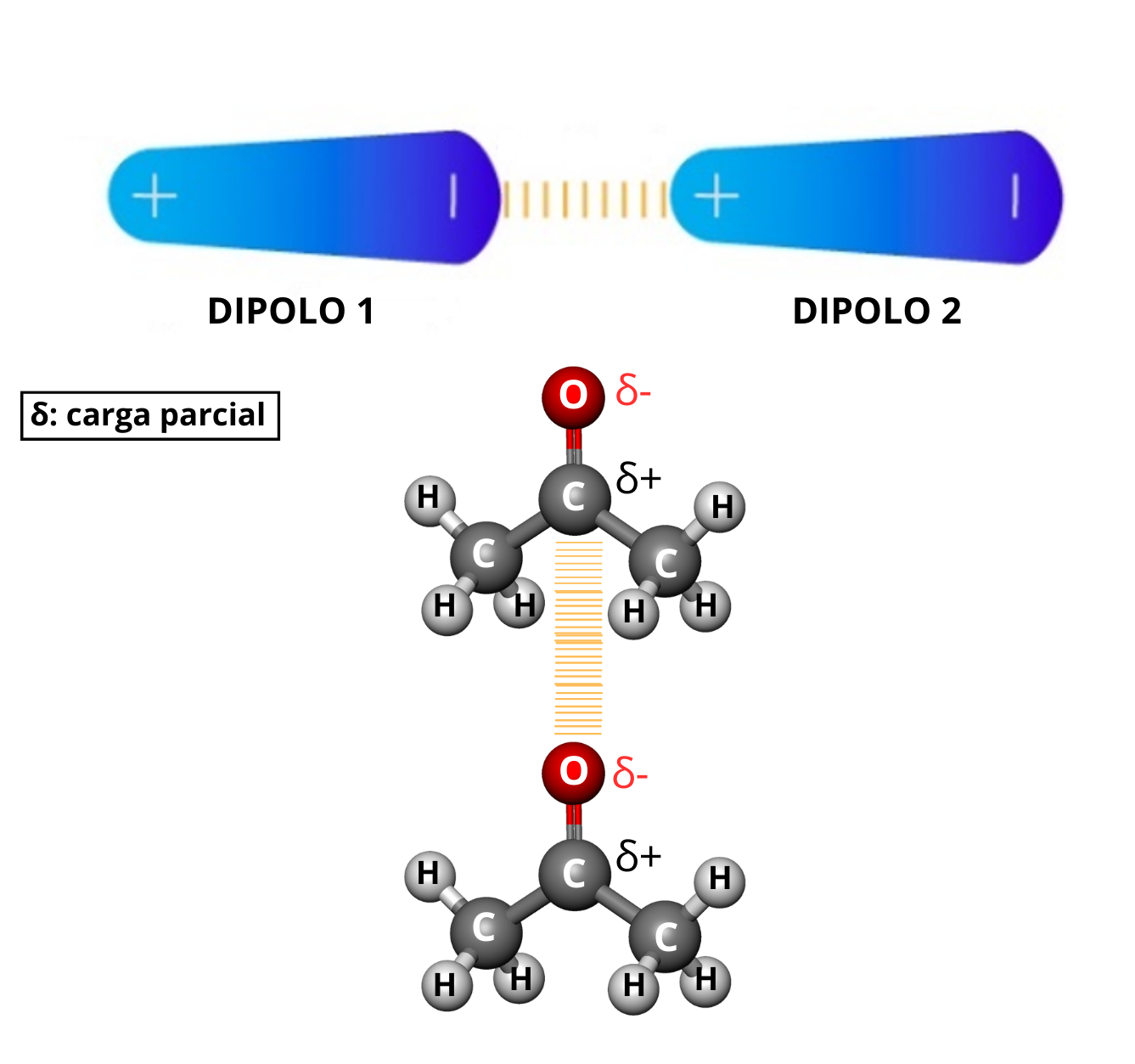
Interacción Dipolo - Dipolo (Fuerzas de Keesom)La interacción dipolo - dipolo se establece cuando una molécula polar (dipolo 1) se aproxima a otra molécula polar (dipolo 2). Esta interacción dipolo-dipolo mantiene unidas a las dos moléculas. La fuerza de la interacción dipolo - . dipolo depende:
|
INTERACCIÓN DIPOLO-DIPOLO (FUERZAD DE DEBYE)
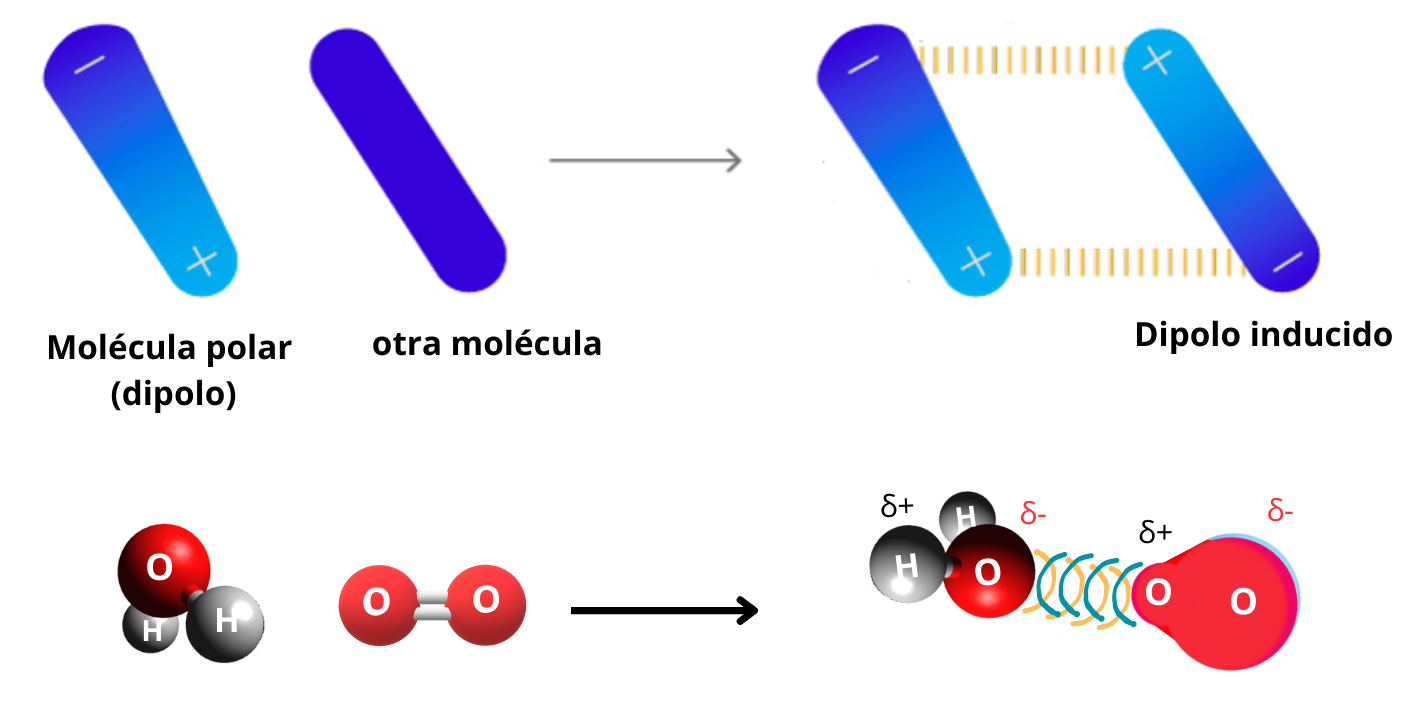
Interacción Dipolo - Dipolo Inducido (Fuerzas de Debye). La interacción dipolo - dipolo inducido se establece cuando una molécula polar (dipolo) se aproxima a otra molécula generando un dipolo en esta otra molécula (dipolo inducido). Esta interacción dipolo-dipolo inducido, mantiene unidas a las dos moléculas. La fuerza de la interacción dipolo - . dipolo inducido depende de:
 |
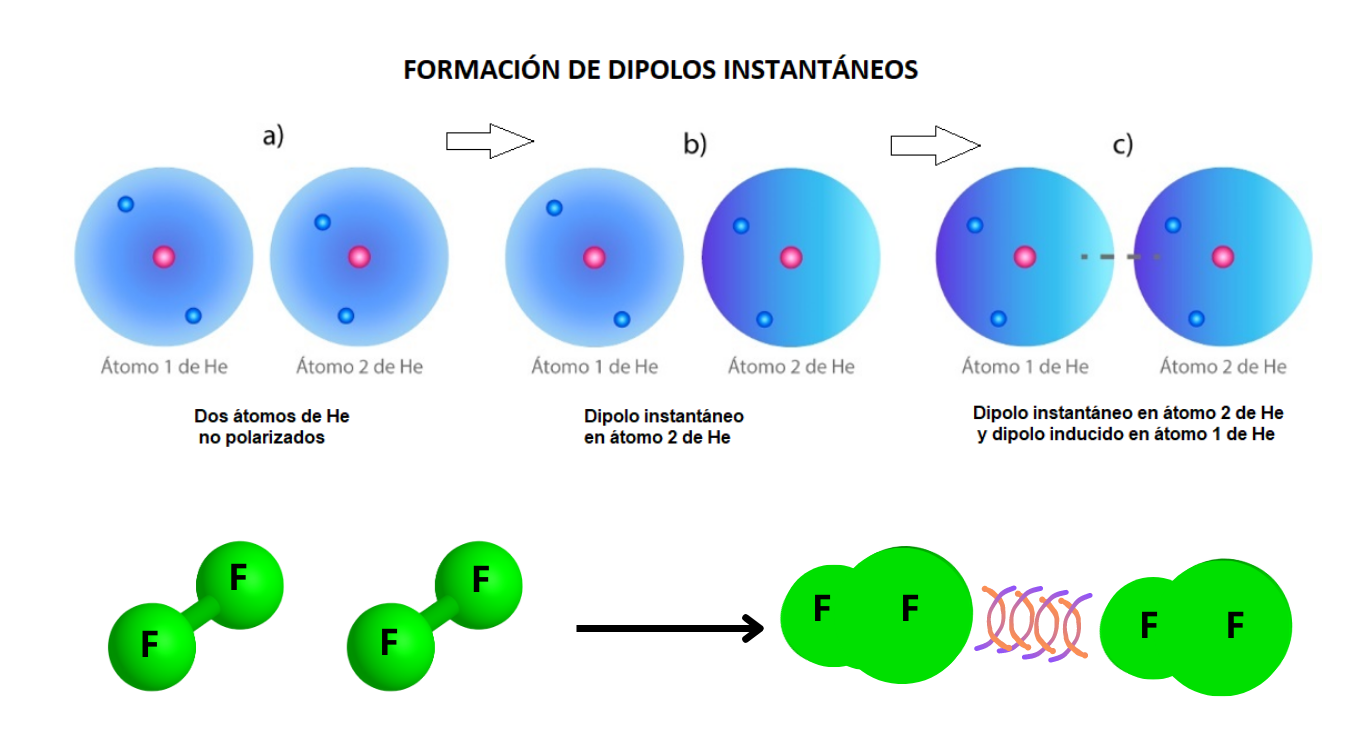
INTERACCIÓNDIPOLO INSTANTÁNEO-DIPOLO INDUCIDO (FUERZAS DE LONDON)zas de London)Interacción Dipolo Instantáneo - Dipolo Inducido (Fuerzas de London). La interacción dipolo instantáneo- dipolo inducido se establece cuando una molécula con un dipolo instantáneo genera un dipolo en otra molécula que está cerca (dipolo inducido). Un dipolo instantáneo se genera por cambios rápidos en la distribución de los electrones en la molécula. Los dipolos instantáneos generan atracciones entre las moléculas incluso cuando las moléculas no son polares.
|
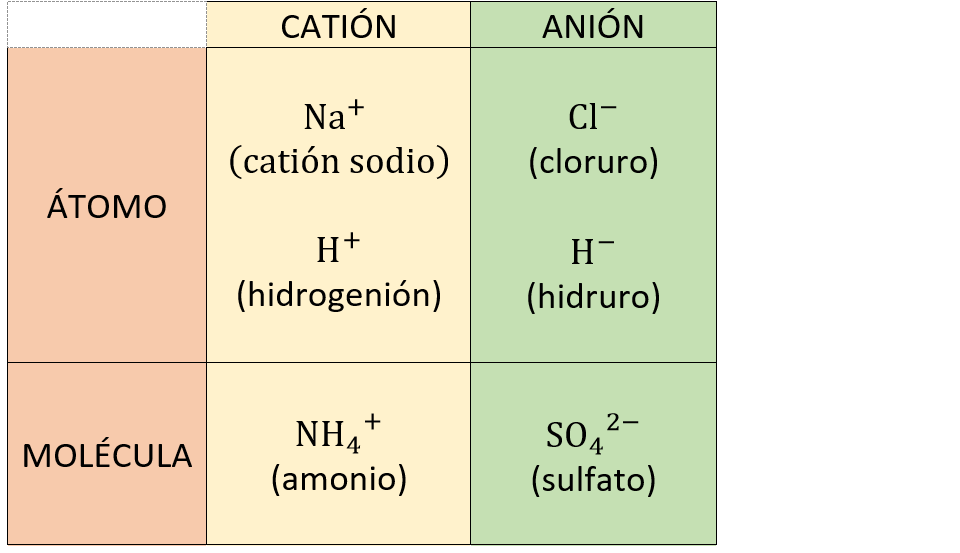
Ion |
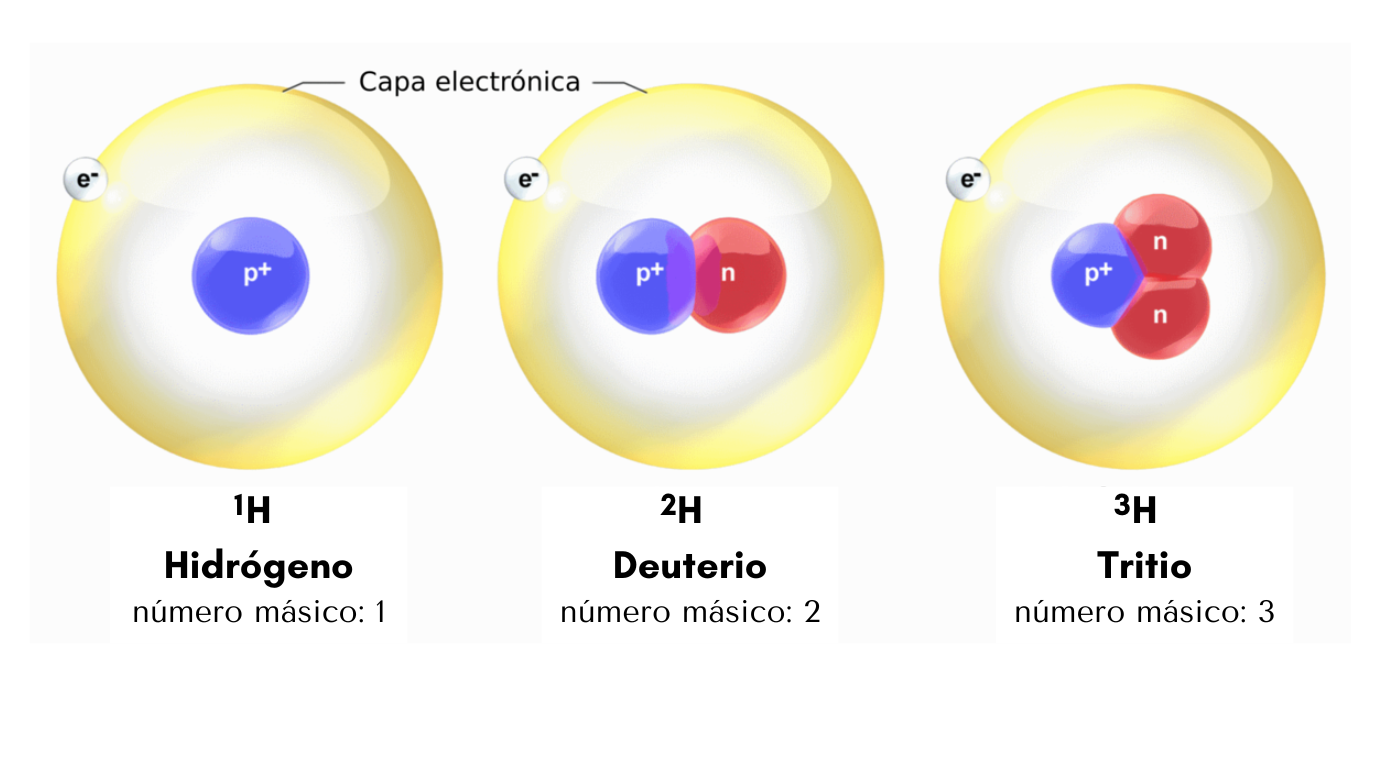
IsótoposLos
isótopos son átomos
de
un mismo elemento con diferente número
másico. Los isótopos tienen igual número de protones pero diferente número de neutrones. Por ejemplo, el elemento hidrógeno posee tres isótopos. El isótopo más abundante es el 1H que tiene un protón. Otro isótopo, el 2H, tiene 1 protón y 1 neutrón. El otro isótopo, el 3H, tiene 1 protón y 2 neutrones.
 |